
| 热化学方程式 | 平衡常数 | |
| 500℃ | 700℃ | |
| ①2H2(g)+CO(g)?CH3OH(g)△H1=a kJ•mol-1 | 2.5 | 0.2 |
| ②H2(g)+CO2(g)?H2O(g)+CO(g)△H2=b kJ•mol-1 | 1.0 | 2.3 |
| ③3H2(g)+CO2 (g)?CH3OH(g)+H2O(g)△H3=c kJ•mol-1 | K3 | 4.6 |
分析 (1)煤的汽化是利用煤与水蒸气反应得到CO与氢气;
(2)①.温度越高平衡常数越小,说明升高温度平衡逆向移动,正反应为放热反应;
反应③=反应①+反应②,则③的焓变=①的焓变+②的焓变;
②.反应③=反应①+反应②,则③的平衡常数=①与②的平衡常数的乘积;
计算此时浓度商Qc,若Qc=K,处于平衡状态,若Qc<K,反应向正反应进行,若Qc>K,反应向逆反应进行,进而判断正逆反应速率相对大小;
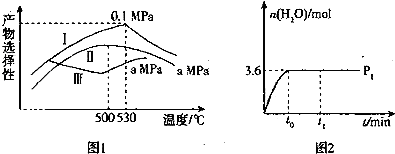
(3)①应根据乙烯的百分比越大、丙烯的百分比越小选择;
②t0时刻,n(H2O)=3.6mol n(CH2=CH2)=1.8mol,设甲醇起始物质的量为x mol,
2CH3OH(g)?CH2=CH2(g)+2H2O(g)
起始量(mol) x 0 0
变化量(mol) 3.6 1.8 3.6
t0时刻量(mol) x-3.6 1.8 3.6
结合甲烷的体积分数列方程计算解答;
体积增大,压强减小,平衡向右移动,导致生成水的量增大,绘制图象时应注意条件改变瞬间水的物质的量没有立即变化.
解答 解:(1)煤的气化是指煤与水蒸气反应生成CO与H2的过程,反应的化学方程式为:C+H2O(g)$\frac{\underline{\;高温\;}}{\;}$CO+H2,
故答案为:C+H2O(g)$\frac{\underline{\;高温\;}}{\;}$CO+H2;
(2)①反应①中,温度越高平衡常数越小,说明升高温度平衡逆向移动,正反应为放热反应,则a<0;
反应③=反应①+反应②,则③的焓变=①的焓变+②的焓变,故c=a+b,
故答案为:<;c=a+b;
②反应③=反应①+反应②,则③的平衡常数=①与②的平衡常数的乘积=2.5×1=2.5;
若反应③是在容积为2L的密闭容器巾进行(500℃)的,测得某一时刻体系内H2、CO2、CH3OH、H2O物质的量分别为6mol、2mol、10,mol、10mol,产生Qc=$\frac{\frac{10}{2}×\frac{10}{2}}{(\frac{6}{2})^{3}×\frac{2}{2}}$=$\frac{25}{27}$<2.5,故此时反应向正反应进行,则甲醇的生成速率大于其消耗速率;
故答案为:2.5;>;
(3)①由图1知,530℃,0.1Mpa时乙烯的选择性最大,为尽可能多地获得乙烯,控制的生产条件为530℃,0.1Mpa;
故答案为:530℃,0.1Mpa;
②t0时刻,n(H2O)=3.6mol n(CH2=CH2)=1.8mol,设甲醇起始物质的量为x mol,
2CH3OH(g)?CH2=CH2(g)+2H2O(g)
起始量(mol) x 0 0
变化量(mol) 3.6 1.8 3.6
t0时刻量(mol) x-3.6 1.8 3.6
所以$\frac{x-3.6}{x-3.6+1.8+3.6}$=10%,解得x=4.2mol
则甲醇的转化率为$\frac{3.6}{4.2}$×100%=85.7%
若在t1 时刻将容器容积快速扩大到原来的2倍,压强减小,后平衡向右移动,导致生成水的量增大,条件改变后瞬间水的物质的量没有立即变化,变化发生后至反应达到新平衡时水的物质的量与时问的关系图为: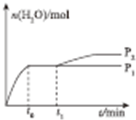 ;
;
故答案为:85.7%; .
.
点评 本题考查化学平衡计算与影响因素、平衡图象、平衡常数、盖斯定律应用等,注意掌握平衡常数的有关应用,题目难度中等.


科目:高中化学 来源: 题型:解答题
 在班级的“元旦晚会”中,小明表演魔术:在桌面上摆4个盛无色液体的高脚杯,他将A高脚杯液体分别倒入其他三个中,看到下列现象:B中液体产生大量气泡变为汽水;C中液体变为红色葡萄酒;D中液体变为“牛奶”(产生大量白色沉淀).
在班级的“元旦晚会”中,小明表演魔术:在桌面上摆4个盛无色液体的高脚杯,他将A高脚杯液体分别倒入其他三个中,看到下列现象:B中液体产生大量气泡变为汽水;C中液体变为红色葡萄酒;D中液体变为“牛奶”(产生大量白色沉淀).查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 实验步骤 | 预期现象和结论 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 序号 | ① | ② |
| PH | 12 | 12 |
| 溶液 | 氨水 | 氢氧化钠溶液 |
| A. | 与AlCl3溶液发生反应的离子方程式均为Al3++3OH-═Al(OH)3↓ | |
| B. | ①溶液的物质的量浓度为0.01mol•L-1 | |
| C. | ①②两溶液分别加水稀释10倍,稀释后溶液的pH:①>② | |
| D. | 等体积的①②两溶液分别与0.01mol•L-1的盐酸完全中和,消耗盐酸的体积:①>② |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某物质的焰色呈黄色,说明该物质一定含有钠元素,不含钾元素 | |
| B. | 氧化钠和过氧化钠和酸均能反应生成盐和水,因此都是碱性氧化物 | |
| C. | 氧化钠和过氧化钠的阴阳离子比前者为1:2,后者为1:1 | |
| D. | 把过氧化钠投入滴有酚酞的水中,溶液先变红后褪色. |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 | |
| B. | 蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口 | |
| C. | 可用酒精萃取碘水中的碘 | |
| D. | 除去淀粉中NaCl杂质,可将混合物加水溶解后,用渗析的方法分离 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 在2L密闭容器内,800℃时反应2NO(g)+O2(g)?2NO2(g)△H<0体系中,n(NO)随时间的变化如下表:
在2L密闭容器内,800℃时反应2NO(g)+O2(g)?2NO2(g)△H<0体系中,n(NO)随时间的变化如下表:| 时间/s | 0 | 10 | 20 | 30 | 40 | 50 |
| n(NO)/mol | 0.20 | 0.10 | 0.08 | 0.07 | 0.07 | 0.07 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
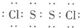 ,其晶体类型为分子晶体.
,其晶体类型为分子晶体.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com