
| A. | 该溶液可由等体积、浓度均为0.1mol•L-1的醋酸和氨水反应得到 | |
| B. | CH3COONH4加人纯水中,水的电离程度不变 | |
| C. | 常温下,电离平衡常数K(CH3 COOH)=K(NH3•H2 O) | |
| D. | 该溶液中c(CH3 COO-)大于同浓度CH3 COONa溶液中的c(CH3 COO-) |
分析 A.等体积、浓度混合后物质的浓度变为原来的一半;
B.弱酸根离子、弱碱阳离子均能促进水的电离;
C.0.1mol•L-1CH3COONH4溶液呈中性,说明醋酸根离子与铵根离子的水解程度相同;
D.醋酸根离子与铵根离子发生相互促进的水解.
解答 解:A.等体积、浓度混合后物质的浓度变为原来的一半,则等体积、浓度均为0.1mol•L-1的醋酸和氨水反应得到1CH3COONH4溶液浓度为0.051mol•L-1,故A错误;
B.弱酸根离子、弱碱阳离子均能促进水的电离,则CH3COONH4加人纯水中,水的电离程度增大,故B错误;
C.0.1mol•L-1CH3COONH4溶液呈中性,说明醋酸根离子与铵根离子的水解程度相同,则对应的酸、碱的电离程度相同,所以二者的电离平衡常数相同,故C正确;
D.CH3COONH4溶液中醋酸根离子与铵根离子发生相互促进的水解,水解程度较大,所以该溶液中c(CH3 COO-)小于同浓度CH3 COONa溶液中的c(CH3 COO-),故D错误.
故选C.
点评 本题考查了盐类水解的应用,弱电解质的电离平衡,弱离子的水解平衡应用,题目难度中等,侧重于基础知识的应用的考查,注意把握盐溶液对水的电离平衡的影响.


科目:高中化学 来源: 题型:填空题
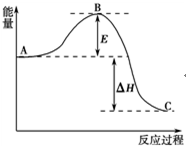 2SO2(g)+O2(g)?2SO3(g)反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1mol SO3(g)的△H=-99kJ•mol-1.请回答下列问题:
2SO2(g)+O2(g)?2SO3(g)反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1mol SO3(g)的△H=-99kJ•mol-1.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 使用催化剂能改变反应限度 | |
| B. | 升高温度,则反应速率减慢 | |
| C. | 四种物质的量浓度相等时,则一定达到了该反应的限度 | |
| D. | 各物质的浓度不再发生变化时,则达到化学反应的限度 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 热稳定性:H2O>H2S>HF | |
| B. | 微粒X2-和Y2+的核外电子排布相同,离子半径:X2-<Y2+ | |
| C. | 第3周期金属都能与氯气发生化合反应 | |
| D. | 第IVA族元素的氧化物都能与NaOH溶液反应生成盐和水 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 $→_{△}^{-H_{2}O}$CH3CH=CHCHO
$→_{△}^{-H_{2}O}$CH3CH=CHCHO +CO$→_{△}^{AlCl_{3},HCl}$
+CO$→_{△}^{AlCl_{3},HCl}$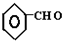

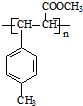 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
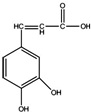
| A. | 分子式为C9H5O4 | |
| B. | 1mol咖啡酸最多可与5mol氢气发生加成反应 | |
| C. | 与溴水既能发生取代反应,又能发生加成反应 | |
| D. | 能与Na2CO3溶液反应,但不能与NaHCO3溶液反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com