
【题目】将4mol A气体和2mol B气体在2L的容器中混合并在一定条件下发生如下反应:2A(g)+B(g)2C(g).若经2s后测得C的浓度为0.6molL﹣1 , 现有下列几种说法:其中正确的是( ) ①用物质A表示的反应的平均速率为0.3molL﹣1s﹣1
②用物质B表示的反应的平均速率为0.6molL﹣1s﹣1
③2s时物质B的浓度为0.7molL﹣1
④2s末,物质A的转化率为70%
A.①④
B.①③
C.②④
D.③④
【答案】B
【解析】解:将 4mol A 气体和 2mol B 气体在 2L 的密闭容器中混合并在一定条件下发生如下反应 2A(g)+B(g)2C(g),若经 2s(秒)后测得 C 的浓度为0.6molL﹣1s﹣1 ,依据化学平衡三段式列式计算
2A(g)+ | B(g) | 2C(g) | |
起始(mol) | 4 | 2 | 0 |
转化(mol) | 1.2 | 0.6 | 1.2 |
平衡(mol) | 2.8 | 1.4 | 2L×0.6mol/L=1.2mol |
①2s后测得A的浓度为0.6molL﹣1,则v(A)= ![]() =0.3mol/(Ls),故①正确;
=0.3mol/(Ls),故①正确;
②用物质B表示反应的平均速率= ![]() mol/(Ls)=0.15mol/(Ls),故②错误;
mol/(Ls)=0.15mol/(Ls),故②错误;
③2s末物质B的浓度= ![]() =0.7molL﹣1;故③正确;
=0.7molL﹣1;故③正确;
④2s末物质A的转化率= ![]() ×100%=30%;故④错误;
×100%=30%;故④错误;
故选B.
【考点精析】本题主要考查了化学平衡的计算的相关知识点,需要掌握反应物转化率=转化浓度÷起始浓度×100%=转化物质的量÷起始物质的量×100%;产品的产率=实际生成产物的物质的量÷理论上可得到产物的物质的量×100%才能正确解答此题.


 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案科目:高中化学 来源: 题型:
【题目】NA为阿伏伽德罗常数的值,下列说法正确的是( )
A. 常温常压下28g N2所含电子数为10NA
B. 46g 钠充分燃烧时转移电子数为2NA
C. 0.1mol/L NH4Cl溶液中NH4+离子数小于0.1NA
D. 密闭容器中3mol NO与1molO2充分反应,剩余气体的分子数为3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用铬铁矿(主要成分可表示为FeO·Cr2O3,还含有Al2O3、MgCO3、SiO2等杂质)为原料制备重铬酸钾晶体(K2Cr2O7)和铁红的流程如下:
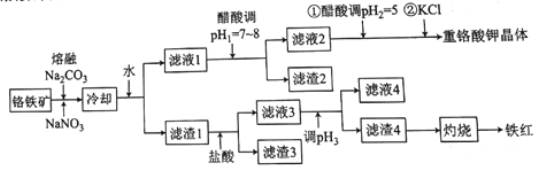
已知:I.常见离子开始生成沉淀和沉淀完全的pH如下表所示:
Fe3+ | Al3+ | Mg2+ | SiO32- | AlO2- | |
开始沉淀的pH | 1.9 | 4.2 | 8.1 | 9.5 | 10.2 |
沉淀完全的pH | 3.2 | 5.3 | 9.4 | 8.0 | 8.5 |
II.熔融Na2CO3条件下主要发生反应:
2FeO·Cr2O3+4Na2CO3+7NaNO3=4Na2CrO4+Fe2O3+4CO2↑+7NaNO2。
(1)熔融Na2CO3条件下还可以得到的副产物为NaAlO2和Na2SiO3,生成这两种副产物的化学方程式为___________________。
(2)滤渣2的主要成分为________(填化学式)。
(3)用醋酸调节pH2=5的目的为__________;若调节的pH过低,NO2-可被氧化为NO3-,其离子方程式为______________。
(4)调节pH2后,加入KCl控制一定条件,可析出K2Cr2O7晶体的可能理由是_______。
(5)调节pH3的范围为______。
(6)检验滤液4中Fe3+是否沉淀完全的方法是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据要求填空:
(1)①常温下,.某溶液中由水电离出的c(OH﹣)=1.0×10﹣10mol/L,该溶液可以是 . (填选项)
A.pH=4的CH3COOH
B.pH=10的NaOH
C.pH=9的 Na2CO3
D.pH=2的 H2SO4
E.pH=4的 NH4Cl
(2)在100℃时,将 100mL 0.1mol/L 的稀H2SO4溶液与 100mL 0.4mol/L的NaOH 溶液混合后,溶液的pH= . (混合时溶液体积变化忽略不计,己知Kw=10﹣12).
(3)常温下,amL0.1mol/L盐酸与bmL0.1mol/L氨水混合,充分反应,若混合后溶液呈中性,则ab (填“<”、“>”或“=”).
(4)常温下,amLpH=3的盐酸与bmLpH=11的氨水混合,充分反应,若a=b,则反应后溶液中离子浓度从大到小的顺序是 .
(5)氯化铝水溶液呈酸性,原因是(用离子方程式表示>: . 把AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是 .
(6)25℃,在0.10mol/LH2S溶液中,通入HCl气体或加入NaOH固体以调节溶液pH,溶液pH与c(S2﹣)关系如下图(忽略溶液体积的变化、H2S的挥发). ①pH=13时,溶液中的 c(H2S)+c(HS﹣)=mol/L.
②某溶液含 0.020mol/LMn2+、0.10mol/LH2S,当溶液pH=时,Mn2+开始沉淀.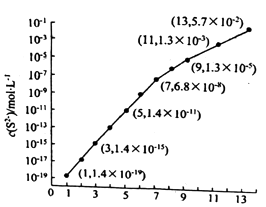
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化学用语表示正确的是
A. 乙烯的比例模型:![]() B. S2-的结构示意图:
B. S2-的结构示意图:![]()
C. KCl的电子式:![]() D. 丙烯的结构简式:CH3CH=CH2
D. 丙烯的结构简式:CH3CH=CH2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】胶体区别于其它分散系的本质特征是
A.胶体分散质粒子直径介于1nm~100nm之间B.胶体能产生丁达尔现象
C.胶体是一种澄清透明的分散系D.胶体可用于净水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定体积的容器中加入1.5mol氙气和7.5mol氟气,于400℃和2633Kpa压强下加热数小时,然后迅速冷至25℃,容器内除得到一种无色晶体外,还余下4.5mol氟气。则所得无色晶体产物中,氙和氟的原子个数之比是 ( )
A.1 :6B.1 :4C.1 :3D.1 :2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组要完成中和热的测定.
(1)实验桌上备有大小两个烧杯、泡沫塑料、泡沫塑料板、胶头滴管、量筒、0.5molL﹣1盐酸、0.55molL﹣1NaOH溶液,实验尚缺少的玻璃用品是 .
(2)①实验中能否用环形铜丝搅拌棒代替环形玻璃搅拌棒?(填“能”或“否”),其原因是 . ②在大、小烧杯之间填满碎泡沫塑料的作用是 .
(3)他们记录的实验数据如表:
实验用品 | 溶液温度 | 中和热 | |||
t1 | t2 | △H | |||
① | 50 mL 0.55 molL﹣1 NaOH溶液 | 50 mL 0.5 molL﹣1 HCl溶液 | 20℃ | 23.3℃ | kJ/mol |
② | 50 mL 0.55 molL﹣1 NaOH溶液 | 50 mL 0.5 molL﹣1 HCl溶液 | 20℃ | 23.5℃ | |
已知:反应后溶液的比热容c为4.18kJ℃﹣1kg﹣1 , 各物质的密度均为1gcm﹣3 . 计算完成上表(保留两位小数).
(4)实验分析 ①若用醋酸代替HCl做实验,测得的中和热的数值(填“偏大”或“偏小”或“无影响”).
②若用60mL 0.5molL﹣1HCl溶液与50mL 0.55molL﹣1NaOH溶液完成实验,与上述实验相比,测得反应放出的热量(填“偏大”或“偏小”或“不变”),中和热(填“偏大”或“偏小”或“不变”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作中,符合操作规范的是
A. 洒出的少量酒精在桌面上燃烧起来,立即用湿抹布盖灭
B. 测定溶液的pH,先用水润湿pH试纸,然后将试纸插入待测液中
C. 为了达到节约药品的目的,将实验后剩余的药品放回原瓶
D. 配制稀硫酸时,将水沿量筒壁慢慢注入浓硫酸中,并不断搅拌
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com