
分析 根据碳酸钙的质量可以计算生成二氧化碳的质量和消耗盐酸的物质的量,进一步可以根据c=$\frac{n}{V}$进行计算求解.
解答 解:设生成二氧化碳的物质的量为xmol,消耗盐酸的物质的量为y,
CaCO3+2HCl═CaCl2+H2O+CO2↑,
100 2mol 1mol
50g y x
则:$\frac{100}{50}=\frac{2}{y}=\frac{1}{x}$,解之得:x=0.5mol,y=1mol,
所以 在标准状况下,产生气体CO2的体积为0.5×22.4=11.2L; 盐酸的物质的量浓度为$\frac{1mol}{0.5L}$=2.00mol/L,
答:(1)在标准状况下,产生气体CO2的体积为11.2L; (2)盐酸的物质的量浓度为2.00mol/L.
点评 本题主要考查学生运用化学方程式进行计算的能力,计算时要注意规范性和准确性.


科目:高中化学 来源: 题型:选择题
| 实际应用 | 相应性质 | |
| A | 用含有酸性重铬酸钾溶液的仪器检验酒后驾车 | 乙醇具有还原性 |
| B | 明矾常用于自来水的净化、杀菌消毒 | 明矾可发生水解生成胶状的Al(OH)3 |
| C | BaSO4可作为造影剂检查肠胃道疾病 | BaSO4难溶于水且不与盐酸反应 |
| D | 过氧化钠可用作呼吸面具中的供氧剂 | Na2O2能与CO2反应生成O2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2 | B. | HY | C. | Y2 O | D. | O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
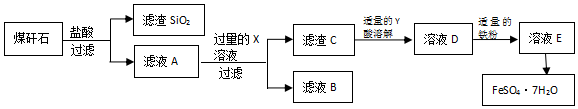
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
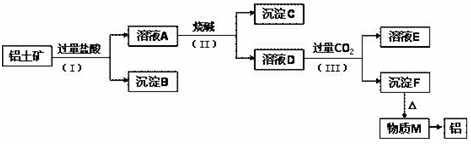
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
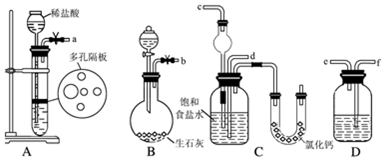
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 室温下,由水电离出c(OH-)=1×10-12 mol•L-1的溶液中:K+、HCO3-、Na+、Cl- | |
| B. | 含有0.1 mol•L-1 Fe2+的溶液中:NH4+、SO42-、H+、NO3- | |
| C. | 使甲基橙变红的溶液中:Cu2+、Mg2+、SO42-、Cl- | |
| D. | 室温下,pH=1的溶液中:Na+、Cl-、K+、CH3COO- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
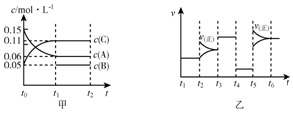 向某密闭容器中加入0.15mol/A、0.05mol/LC和一量的B三种气体.一定条件下发生反应,各物质浓度随时间变化如图中甲图所示[t0时c(B)未画出,t1时增大到0.05mol/L].乙图中t2时刻后改变反应条件,平衡体系中正、逆反应速率随时间变化的情况.
向某密闭容器中加入0.15mol/A、0.05mol/LC和一量的B三种气体.一定条件下发生反应,各物质浓度随时间变化如图中甲图所示[t0时c(B)未画出,t1时增大到0.05mol/L].乙图中t2时刻后改变反应条件,平衡体系中正、逆反应速率随时间变化的情况.| T1~t2 | T3~t4 | T4~t5 | T6~t |
| K1 | K2 | K3 | K4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com