
【题目】能源在人类生活中应用广泛。回答下列问题:
(1)氢气燃烧时放出大量的热,这是由于反应物的总能量____生成物的总能量(选填“大于”“小于”或“等于”,下同),从化学反应的本质角度来看,是由于断裂反应物中的化学键吸收的总能量_____形成产物的化学键释放的总能量。
(2)H2被认为是21世纪矿物燃料的理想能源,每克氢气和汽油燃烧放出的热量分别为55kJ和46kJ。汽油可由石油经___和____获得;请分析氢气作为能源替代汽油的优势:_____;____(写两点)。
(3)在氢氧碱性燃料电池中,负极发生反应的电极反应式:___,正极的电极反应式为____。若反应后得到5.4g液态水,此时氢氧燃料电池转移的电子数为____。
(4)如图所示的装置,在盛有水的烧杯中,铁圈和银圈的连接处吊着一根绝缘的细丝,使之平衡。小心地往烧杯中央滴入CuSO4溶液。

片刻后可观察到的现象是(指悬吊的金属圈)____。
A.铁圈和银圈左右摇摆不定 B.保持平衡状态不变
C.铁圈向下倾斜 D.银圈向下倾斜
(5)铁及铁的化合物应用广泛,如FeCl3可用作催化剂、印刷电路铜板腐蚀剂和外伤止血剂等。
①写出FeCl3溶液腐蚀印刷电路铜板的离子方程式_____。
②若将①中的反应设计成原电池,写出负极的电极反应式____。
【答案】大于 小于 分馏 裂化 氢气燃烧产物为水,不污染环境 单位质量的氢气燃烧放出的热量更多 H2-2e-+2OH-=2H2O O2+4e-+2H2O=4OH- 0.6NA D 2Fe3++Cu=2Fe2++Cu2+ Cu-2e-=Cu2+
【解析】
(1)放热反应是反应物的总能量大于生成物的总能量的反应;
(2)石油分馏和裂化可得到汽油;氢气是清洁燃料;
(3)在氢氧碱性燃料电池中,负极是氢气失电子生成水;正极是氧气得电子生成氢氧根离子。
(4)如图所示的装置,铁圈和银圈、硫酸铜溶液构成原电池;
(5)①FeCl3溶液与铜反应生成氯化亚铁和氯化铜;
②若将①中的反应设计成原电池,铜是负极,负极是铜失电子生成铜离子;
(1)反应物的总能量大于生成物的总能量的反应为放热反应;氢气燃烧放热,这是由于反应物的总能量大于生成物的总能量;
(2)石油分馏和裂化可获得汽油;氢气作为能源替代汽油的优势是:氢气燃烧产物为水,不污染环境 ;单位质量的氢气燃烧放出的热量更多。
(3)在氢氧碱性燃料电池中,负极是氢气失电子生成水,负极反应式是H2-2e-+2OH-=2H2O,正极是氧气得电子生成氢氧根离子,正极反应式为O2+4e-+2H2O=4OH-。氢氧燃料电池总反应为2H2+O2=2H2O,5.4g水的物质的量是0.3mol,若反应后得到5.4g液态水,此时氢氧燃料电池转移的电子数为0.6NA。
(4)如图所示的装置,铁圈和银圈、硫酸铜溶液构成原电池,铁负极,Fe-2e-=Fe2+,铁溶解,质量减轻,银是正极Cu2++2e-=Cu,银极质量增大,所以银圈向下倾斜,选D;
(5)①FeCl3溶液与铜反应生成氯化亚铁和氯化铜,离子方程式是2Fe3++Cu=2Fe2++Cu2+。
②若将①中的反应设计成原电池,铜是负极,负极是铜失电子生成铜离子,负极的电极反应式是Cu-2e-=Cu2+。


科目:高中化学 来源: 题型:
【题目】有容积不同的X、Y两密闭容器,X中充满CO气体,Y中充满CH4、O2、N2的混合气体,同温同压下测得两容器中气体密度相同。下列叙述中不正确的是
A.Y容器中CH4、O2、N2的质量之比可以为1∶6∶3
B.Y容器中CH4、O2、N2的物质的量之比一定为1∶3∶6
C.两容器中所含气体分子数一定不同
D.两容器中所含气体的质量一定不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从元素化合价和物质类别两个角度学习、研究物质的性质,是一种行之有效的方法。以下是氮元素形成物质的价类二维图的及氮的循环的部分信息。
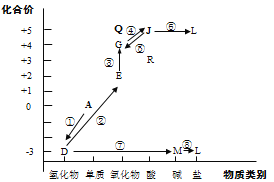
(1)①是一种人工固氮的重要途径,该反应的化学方程式是__________。
(2)②的化学方程式是__________。
(3)⑤的化学方程式是(任写一种)__________。
(4)R可与 NaOH溶液反应:HNO2+NaOH=NaNO2+H2O,该反应体现了R(HNO2)的_____性。
(5)Q的化学式是_______,Q属于酸性氧化物,写出Q与水反应的化学方程式________。
(6)L在水体中过多蓄积会导致水体富营养化。将水体调节为酸性后加入适量NaClO,可将L中阳离子转化为无污染气体以去除。写出L与NaClO反应的离子方程式_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】美托洛尔可治疗各型高血压及作血管扩张剂,它的一种合成路线如下:

已知:![]() +
+![]()
![]()
![]() +HCl
+HCl
(1)A的化学名称是 _________,B的结构简式为__________,美托洛尔中含氧官能团的名称是_____________。
(2)A合成B的反应中,加人K2CO3的作用可能是 _________。
(3)B合成C的反应类型是________ 。
(4)F生成G的化学方程式为________ 。
(5)氯甲基环氧乙烷(![]() ) 是合成有机化合物的重要原料,实验室检验卤代烃中氯原子的常用试剂是______。
) 是合成有机化合物的重要原料,实验室检验卤代烃中氯原子的常用试剂是______。
(6)芳香族化合物M是F的同分异构体.则符合下列条件的M共有___种(不含立体异构)。
①苯环上只有2个取代基
②1molM与足量 Na 充分反应能生成1mol H2
③能与FeCl3溶液发生显色反应。
其中核磁共振氢谱为5组峰同分异构体的结构简式为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用如图装置可以验证非金属性的变化规律。

(1)仪器A的名称为________,干燥管D的作用是________________。
(2)已知在常温下,高锰酸钾和浓盐酸反应能生成氯气。实验室中现有药品Na2S溶液、KMnO4、浓盐酸、MnO2,请选择合适药品设计实验验证氯的非金属性大于硫的;装置A、B、C中所装药品分别为________、________、________,装置C中的实验现象为_________________,离子方程式为______。
(3)若要证明非金属性:S>C>Si,则A中加________、B中加Na2CO3、C中加________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮、硫、氯及其化合物是中学化学重要的组成部分。
(1)氨气燃料电池使用的电解质溶液是KOH溶液,电池反应为:4NH3+3O2=2N2+6H2O。该电池负极的电极反应式为____;用该电池进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼,以CuSO4溶液为电解质溶液,下列说法正确的是____。
a.电能全部转化为化学能
b.SO42﹣的物质的量浓度不变(不考虑溶液体积变化)
c.溶液中Cu2+向阳极移动
d.利用阳极泥可回收Ag、Pt、Au等金属
e.若阳极质量减少64g,则转移电子数为2NA个
(2)①将SO2通入到BaCl2溶液中,出现了异常现象,看到了明显的白色沉淀,为探究该白色沉淀的成分,他设计了如下实验流程:所得悬浊液![]() 白色沉淀
白色沉淀![]() 观察现象并判断,则试剂A的化学式为_____。实验表明,加入试剂A后,白色沉淀未见溶解,产生该白色沉淀的离子方程式是____。
观察现象并判断,则试剂A的化学式为_____。实验表明,加入试剂A后,白色沉淀未见溶解,产生该白色沉淀的离子方程式是____。
②利用如图所示电化学装置吸收工业尾气中SO2,阴极上生成Cu。写出装置中阳极的电极反应式_____。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组采用如图所示装置,对浓硝酸与木炭的反应进行探究(已知:4HNO3![]() 4NO2↑+O2↑+2H2O)。
4NO2↑+O2↑+2H2O)。
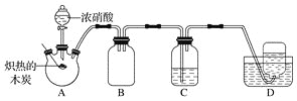
请回答下列问题:
(1)检查装置气密性后,将燃烧匙中的木炭在酒精灯上加热至炽热状态,伸入三颈烧瓶中,生成的气体的颜色为__,产生该气体的反应的化学方程式是__。
(2)装置C中盛有足量Ba(OH)2溶液,炽热的木炭与浓硝酸反应后可观察到C中出现白色沉淀,该白色沉淀为__(填化学式)。
(3)装置B的作用是__。
(4)装置D中收集到了无色气体,有同学认为是NO,还有同学认为是O2。
①下列对该气体的检验方法合适的是__(填字母)。
A.敞口观察装置D中集气瓶内气体的颜色变化
B.将湿润的蓝色石蕊试纸伸入集气瓶内,观察蓝色石蕊试纸是否变红
C.将带火星的木条伸入集气瓶中,观察木条是否复燃
②如果D中集气瓶内收集到的无色气体是氧气,则氧气的来源是__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在给定条件下,下列选项所示的物质间转化均能实现的是( )
A. NaCl(aq)![]() Cl2(g)
Cl2(g)![]() FeCl2(s)
FeCl2(s)
B. AlCl3(aq)![]() Al(OH)3(s)
Al(OH)3(s)![]() Al2O3(s)
Al2O3(s)
C. S(s)![]() SO3(g)
SO3(g)![]() H2SO4(aq)
H2SO4(aq)
D. N2(g)![]() NH3(g)
NH3(g)![]() NaHCO3(s)
NaHCO3(s)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是分离混合物时常用的仪器,可以进行的混合物分离操作分别是()
![]()
A.蒸馏、过滤、萃取、蒸发B.蒸馏、蒸发、萃取、过滤
C.萃取、过滤、蒸馏、蒸发D.过滤、蒸发、萃取、蒸馏
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com