
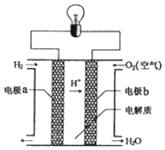
 氢氧燃料电池可以使用在航天飞机上,其反应原理示意图如图.下列有关氢氧燃料电池的说法不正确的是( )
氢氧燃料电池可以使用在航天飞机上,其反应原理示意图如图.下列有关氢氧燃料电池的说法不正确的是( )| A. | 该装置将化学能转化为电能 | |
| B. | 为了增加灯泡亮度,可以将电极碳棒变得多粗糙多孔 | |
| C. | 电子迁移方向:电极a→灯泡→电极b→电解质溶液→电极a | |
| D. | 该电池的总反应:2H2+O2═2H2O |
分析 氢氧燃料电池中,氢气易失电子发生氧化反应,所以通入氢气的电极是负极,氧气易得电子发生还原反应,所以通入氧气的电极是正极;氢氧燃料电池的产物是水,据此分析解答.
解答 解:A.燃料电池中,将化学能转化为电能,故A正确;
B.将电极碳棒变得多粗糙多孔,增加接触面积,可以加快反应速率增加灯泡亮度,故B正确;
C.外电路中电子由负极到正极,但不能通过电解质溶液,故C错误;
D.氢氧燃料电池的正负极反应物分别为氢气和氧气,该电池的总反应:2H2+O2=2H2O,故D正确.
故选C.
点评 本题考查了燃料电池,侧重于原电池原理的考查,题目难度不大,注意氢氧燃料电池的反应产物为水,环保无污染.


科目:高中化学 来源: 题型:选择题
| A. | 只有①③④⑤ | B. | 只有①④⑤ | C. | 只有②③④⑤ | D. | 只有②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
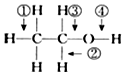
| A. | 和金属钠反应时键④断裂 | |
| B. | 和氢溴酸反应时键②断裂 | |
| C. | 和浓硫酸共热140℃时键③或键④断裂;170℃时键①③断裂 | |
| D. | 在Ag催化下和O2反应键②④断裂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 滴定终点时,溶液变为红色 | |
| B. | 该滴定法需在碱性条件下进行 | |
| C. | AgBr(s)+SCN-?AgSCN(s)+Br-(aq)的平衡常数K=0.77 | |
| D. | 该水样中溴离子浓度为:c(Br-)=$\frac{({c}_{1}{V}_{1}-{c}_{2}{V}_{2})}{25.00}$mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:A>B>D>C | B. | 原子序数:b>a>c>d | ||
| C. | 离子半径:D(n+1)->Cn->An+>B(n+1)+ | D. | 金属性:B>A,非金属性:D>C |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 不能和氢氧化钠溶液发生反应 | |
| B. | 分子中N≡C键的键长大于C-C键的键长 | |
| C. | 该分子与H2O2分子的空间构型类似 | |
| D. | 分子中原子的最外层均满足8电子结构 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙醇在加热的条件下,可以使黑色的氧化铜变红,生成具有特殊气味的乙醛 | |
| B. | 葡萄糖在一定条件下可以水解生成乙醇和二氧化碳 | |
| C. | 油脂和乙酸乙酯都属于酯类物质,碱性下水解都称之为皂化反应 | |
| D. | 豆浆中富含大豆蛋白,煮沸后蛋白质即水解生成氨基酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
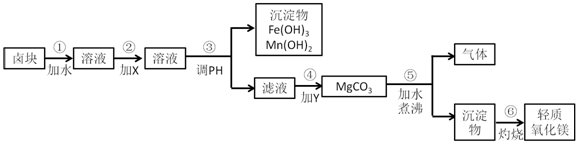
| 物质 | 价格/(元•吨-1) |
| 漂液(含25.2%NaClO) | 450 |
| 双氧水(30%H2O2) | 2400 |
| 烧碱(含98%NaOH) | 2100 |
| 纯碱(含99.5%Na2CO3) | 600 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 取c(H+)=0.01mol/L的盐酸和醋酸各100mL,分别稀释2倍后,再分别加入0.03g锌粉,在相同条件下充分反应,醋酸与锌反应的速率大 | |
| B. | 含等物质的量的NaHC2O4和Na2C2O4的溶液中存在:2c(Na+)=3[c(HC2O4-)+c(C2O42-)+c(H2C2O4)] | |
| C. | 25℃时,某溶液中由水电离出的c(H+)=10-amol/L,若a>7时,该溶液pH一定为14-a | |
| D. | 25℃时,pH=11 NaOH溶液和pH=3 CH3COOH混合,若溶液显酸性,则所得溶液中离子浓度可能为c(CH3COO-)>c(H+)>c(Na+)>c(OH-) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com