
2009��10��16�գ���11��ȫ�˻Ὣ��ɽ�����Ͼٰ졣���д�ʩ�����ڼ��Ͻ��ܼ��š����ƻ����������� ( )
�� �����Ļ�������վ���밲װ����������ʩ���Լ��ٻ������������SO2�ŷ�
�� �������С���������ӿ��з����ö�����̼�ϳɵľ�̼������ɽ�������
�� ����ȼ�����Ҵ����ͣ��Լ�������β����Ⱦ
�� ��չ��̼���á�ѭ�����ã��ƹ������̫���ܡ����ܵij�������ϵͳ
�� ʹ������ø���������ˮ�е��л��ʹ��������δ���������������
A�� �٢ڢۢ� B���٢ڢ� C���٢ڢܢ� D���ۢܢ�
![]()
![]()
![]()
 ѧ���쳵�����ּ��ں�����ҵϵ�д�
ѧ���쳵�����ּ��ں�����ҵϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| [CH3OH] |
| [CO][H2]2 |
| [CH3OH] |
| [CO][H2]2 |
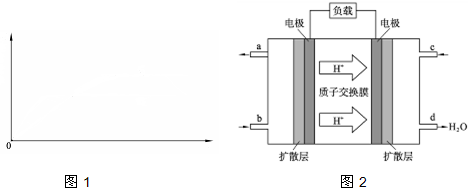
| b-a-4c |
| 2 |
| b-a-4c |
| 2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2011-2012ѧ�����ɹŰ�ͷ��ʮ���и߶���ѧ����ĩ���Ի�ѧ�Ծ� ���ͣ������
��8�֣���2009��10��16�յ�ʮһ��ȫ�˻��ڼ��Ͼ��У�ȫ�˻�ʹ�õĻ���ȼ���DZ��顣
��1����֪11g������ȫȼ������CO2��Һ̬ˮʱ�ų�������Ϊ555kJ����д������ȼ���ȵ��Ȼ�ѧ����ʽ
(2)ij�¶��£���ˮ�е�c��H+��=2.0��10-7mol/L�����¶Ȳ��䣬����ϡ����ʹc��H+��=5.0��10-6mol/L�������Һ����ˮ�������c��OH-��Ϊ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012-2013ѧ��㶫ʡ������һ��8���¿������ۺϻ�ѧ�Ծ��������棩 ���ͣ������
��16�֣��״���һ�ֿ�������Դ�����п�����Ӧ�õĹ���ǰ������ҵ��һ��ɲ������·�Ӧ���ϳɼ״��� CO(g)+2H2(g)
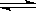 CH3OH(g) ��H<
0��
CH3OH(g) ��H<
0��
��1��������Ӧ��ƽ�ⳣ������ʽΪK= �������й�˵����ȷ����________
a�����¡����������£������ڵ�ѹǿ�������仯����淴Ӧ�ﵽƽ��
b��һ�������£�H2������������CO���������ʵ�2��ʱ���淴Ӧ�ﵽƽ��
c����������������䣬�����¶ȿ����CO��ת����
d��ʹ�ú��ʵĴ��������̴ﵽƽ���ʱ�䲢���CH3OH�IJ���
��2������������ͬʱ����T1��T2��T1< T2��������ͬ�¶��¿��淴Ӧ�ﵽƽ�⣬�뻭��CO��ת������ʱ��仯��ʾ��ͼ��

��3����֪�ڳ��³�ѹ�£�
�� 2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) ��H �� -a kJ��mol-1
�� 2CO(g)+O2(g)=2CO2(g) ��H �� -b kJ��mol-1
�� H2O(g)= H2O(l) ��H�� -c kJ��mol-1
�� CH3OH(l)+ O2(g) = CO (g) + 2H2O(l) ��H��______________kJ��mol-1��
��4��2009��10�£��й���ѧԺ����Ӧ�û�ѧ�о����ڼ״�ȼ�ϵ�ؼ�����������ͻ�ƣ���װ�����Ժ�����ؼ�����ʽ��ѡ��״�ȼ�ϵ�صĹ���ԭ����ͼ��ʾ��
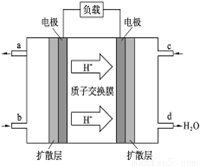
C�������ĵ缫��ӦʽΪ:___________________________������һ��ʱ���6.4 g�״���ȫ��Ӧ����CO2ʱ����______NA�����ӷ���ת�ơ�
��H��1 C��12 O��16��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ����ĩ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com