考点:物质分子中的原子个数计算,阿伏加德罗定律及推论,物质的量的相关计算
专题:阿伏加德罗常数和阿伏加德罗定律
分析:(1)根据m=n×M,V=n×Vm进行计算;
(2)根据m=n×M进行计算.
解答:
(1)在标准状况下,①4g H
2的物质的量为
=2mol;原子数为2×2=4mol;体积为2×22.4=44.8L;
②33.6L CH
4的物质的量为
=1.5mol;原子数为1.5×5=7.5mol;质量为1.5×16=24g;
③1mol H
2O的物质的量为1mol;原子数为1×3=3mol;质量为18g;
④3.01×10
23个O
2的物质的量为
=0.5mol;原子数为0.5×2=1mol;质量为0.5×32=16g;体积为0.5×22.4=11.2L,
故含分子数最多的是①;含原子数最少的是④;质量最大的是②;体积最小的是③;密度由大到小的顺序为③>④>②>①;
故答案为:①;④;②;③;③>④>②>①;
(2)含有相同氧原子数的CO和CO
2,其物质的量比为
:=2:1;质量比为2×28:1×44=14:11;原子数比为2×2:1×3=4:3,
故答案为:2:1;14:11;4:3.
点评:本题考查阿伏伽德罗常数及相关物质的量的计算,数据较多,难度不大.



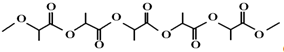 (结构简式)可被人体吸收,常作为外科缝合手术的材料,该物质由下列哪种物质聚合而成( )
(结构简式)可被人体吸收,常作为外科缝合手术的材料,该物质由下列哪种物质聚合而成( )