
下列说法正确的是( )
A.0.1 mol/L (NH4)2SO4溶液中的c(NH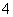 )<c(SO
)<c(SO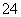 )
)
B.相同温度下,0.6 mol/L氨水溶液与0.3 mol/L氨水溶液中c(OH-)之比是21
C.向0.1 mol/L NaNO3溶液中滴加盐酸使溶液pH=5,此时混合液中的c(Na+)=c(NO )
)
D.常温下,向醋酸钠溶液中加入适量醋酸,使混合液的pH=7,此时混合液中c(Na+)>c(CH3COO-)
 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案科目:高中化学 来源: 题型:
一定温度下,在固定体积的密闭容器中发生下列反应:2HI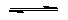 H2+I2。若c(HI)由0.1mol·L-1降到0.07mol·L-1时,需要15s,那么c(HI)由0.07mol·L-1降到0.05mol·L-1时,所需反应的时间为 ( )
H2+I2。若c(HI)由0.1mol·L-1降到0.07mol·L-1时,需要15s,那么c(HI)由0.07mol·L-1降到0.05mol·L-1时,所需反应的时间为 ( )
A. 5s B. 10s C. 大于10s D. 小于10s
查看答案和解析>>
科目:高中化学 来源: 题型:
下列金属冶炼的反应原理,错误的是 ( )
A.MgCl2(熔融)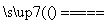 Mg+Cl2↑
Mg+Cl2↑
B.Al2O3+3H2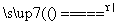 2Al+3H2O
2Al+3H2O
C.Fe3O4+4CO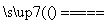 3Fe+4CO2
3Fe+4CO2
D.2HgO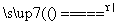 2Hg+O2↑
2Hg+O2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
某废金属屑中主要成分为Cu、Fe、Al,还含有少量的铜锈[Cu2(OH)2CO3]、少量的铁锈和少量的氧化铝,用上述废金属屑制取胆矾(CuSO4·5H2O)、无水AlCl3和铁红的过程如下图所示:
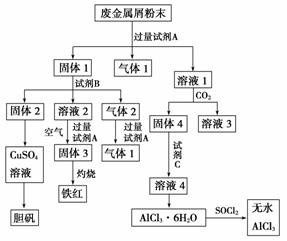
请回答:
(1)在废金属屑粉末中加入试剂A,生成气体1的反应的离子方程式是________________________________________________________________________
________________________________________________________________________。
(2)溶液2中含有的金属阳离子是__________;气体2的成分是__________。
(3)溶液2转化为固体3的反应的离子方程式是________________________________
________________________________________________________________________。
(4)利用固体2制取CuSO4溶液有多种方法。
①在固体2中加入浓H2SO4并加热,使固体2全部溶解得CuSO4溶液,反应的化学方程式是_______________________________________________ _____________________。
_____________________。
②在固体2中加入稀H2SO4后,通入O2并加热,使固体2全部溶解得CuSO4溶液,反应的离子方程式是_________________________________________________________
________________________________________________________________________。
(5)溶液1转化为溶液4过程中,不在溶液1中直接加入试剂C,理由是________________________________________________________________________
________________________________________________________________________。
(6)直接加热AlCl3·6H2O不能得到无水AlCl3。SOCl2为无色液体,极易与水反应生成HCl和一种具有漂白性的气体。AlCl3·6H2O与SOCl2混合加热制取无水AlCl3,反应的化学方程式是______________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是( )
A.pH=5.2的CH3COOH与CH3COONa混合溶液中,c(Na+)>c(CH3COO-)
B.在滴有酚酞溶液的氨水里加入盐酸至溶液恰好无色,则此时溶液的pH=7
C.若100 mL pH=11的NaOH溶液与10 mL盐酸混合后溶液的pH=7,则盐酸溶液的pH=2
D.某醋酸溶液的pH=3,将此溶液稀释10倍后溶液的pH=4
查看答案和解析>>
科目:高中化学 来源: 题型:
我们已经知道,pH表示溶液中c(H+)的负对数,同样也可以定义pOH表示溶液中c(OH-)的负对数,即pOH=-lg c(OH-),温度T时水的离子积常数用KW表示,此温度下不能判定溶液呈中性的依据是( )
A.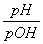 =1 B.pOH=-lg
=1 B.pOH=-lg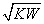
C.c(H+)=10-pOH D.pH+pOH=lg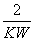
查看答案和解析>>
科目:高中化学 来源: 题型:
化学已渗透到人类生活的各个方面。下列说法不正确的是
A.凡含有食品添加剂的食物对人体健康均有害,不可食用
B.地沟油的主要成分是高级脂肪酸甘油酯,处理后可用于制肥皂
C.钻石、水晶、刚玉都是人们熟知的宝石,但其化学成分不同
D.低盐低脂饮食是目前大力提倡的健康饮食方法,可有效预防高血压等疾病
查看答案和解析>>
科目:高中化学 来源: 题型:
.将标准状况下的a L HCl(g)溶于1000g水中,得到的盐酸密度为bg·cm-3,则该
盐酸的物质的量浓度是
A. 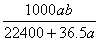 mol/L B.
mol/L B. 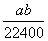 mol/L
mol/L
C.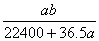 mol/L D.
mol/L D. 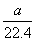 mol/L
mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
A+、B2+、C-、D2-四种离子具有相同电子层结构。现有以下排列顺序:
①B2+>A+>C->D2-;②C->D2->A+>B2+;③B2+>A+>D2->C-;④D2->C->A+>B2+ 。四种离子的半径由大到小以及四种元素原子序数由大到小的顺序分别是
A.①④ B.④① C.②③ D.③②
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com