
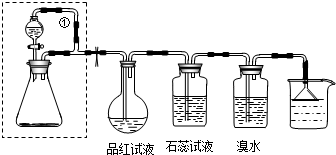


科目:高中化学 来源: 题型:
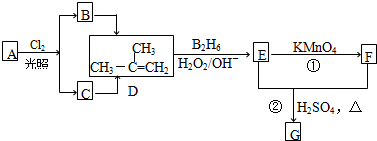
| ||
| H2O2/OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、石油分馏可以获得重要的有机化工原料乙烯 |
| B、乙醇、乙酸、乙酸乙酯可用饱和氢氧化钠溶液鉴别 |
| C、乙烷和苯所含的碳碳键不同,但都能发生氧化反应和取代反应 |
| D、糖类、油脂和蛋白质都是人体必需的营养物质,它们的组成元素相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
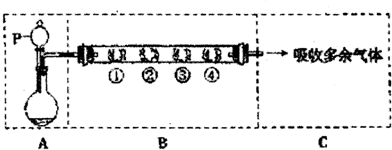
| B中棉花的位置 | ① | ② | ③ | ④ |
| 所 蘸 试剂 | 石蕊试纸 | 品红溶液 | 淀粉和碘水混合物 | 氢硫酸 |
| 现象 | 褪色 | 浅黄色固体 | ||
| 体现SO2性质 | 水溶液显酸性 | 漂白性 | 氧化性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
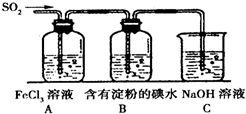 为探究SO2气体的还原性某兴趣小组设计了如装置图:
为探究SO2气体的还原性某兴趣小组设计了如装置图:查看答案和解析>>
科目:高中化学 来源: 题型:
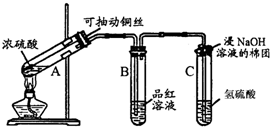
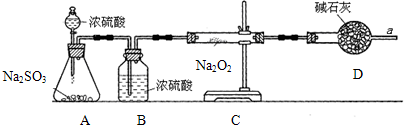
查看答案和解析>>
科目:高中化学 来源: 题型:
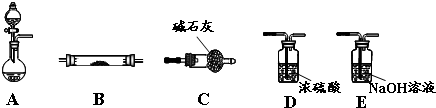
查看答案和解析>>
科目:高中化学 来源: 题型:
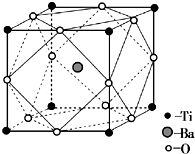 钛被誉为“未来世纪的金属”.试回答下列问题:
钛被誉为“未来世纪的金属”.试回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com