(2011?武汉模拟)某化学兴趣小组的同学通过査阅资料,获得了草酸的一些信息,整理出下表:
| 结构简式 |
HOOH-COOH |
| 溶解性 |
能溶于水,易溶于乙醇 |
| 特性 |
大约在157℃升华(175℃以上发生分解) |
| 化学性质 |
H2C2O4+Ca(OH)2═CaC2O4↓+2H2O |
| HOOC-COOHCO2↑+CO+H2O↑ |
| 2KMnO4+5H2C2O4+3H2SO4═KSO4+2MnSO4+10CO2↑2O |
(1)该组同学欲通过实验验证草酸受热分解产物中的CO
2和CO(装置符合气密性要求,其它试剂可自选).
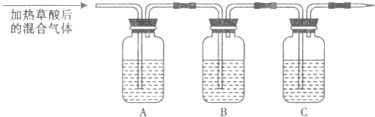
①填写表中空白.
②简述检验CO的实验方法和实验现象.
在C处后尖嘴管点燃气体,火焰呈蓝色,再用一个内壁附着澄清石灰水的烧杯罩在火焰上,烧杯内壁的石灰水变浑浊
在C处后尖嘴管点燃气体,火焰呈蓝色,再用一个内壁附着澄清石灰水的烧杯罩在火焰上,烧杯内壁的石灰水变浑浊
(2)实验室常用草酸钠测定KMnO
4溶液的浓度.
①准确称取2.680g草酸钠,溶于稀硫酸和水制成100.0mL溶液,每次取20.00mL溶液于锥形瓶中;将待测KMnO
4溶液置于
酸式
酸式
(填“酸式”或“碱式“)滴定管中进行滴定.重复上述滴定操作三次,实验数据如表所示.
|
滴定前均为 |
第一次终点 |
第二次终点 |
第三次终点 |
| 滴定管液面刻度 |
0.00mL |
20.02mL |
21.00mL |
19.98mL |
待测KMnO
4溶液的物质的量浓度为
0.08000 mol/L
0.08000 mol/L
.
②将酸性高锰酸钾溶液和草酸溶液混合后,发现开始时溶液褪色不明显,但不久迅速褪色.针对该实验现象,某同学认为KMnO
4溶液与H
2C
2O
4溶液反应是放热反应,导致溶液温度升高,反应速率加快.你猜想还有可能是
催化剂(或Mn2+的催化作用)
催化剂(或Mn2+的催化作用)
的影响.若用实验证明你的猜想,除高锰酸钾溶液、草酸溶液、稀硫酸外,还需要选择的合理试剂是
硫酸锰(或MnSO4)
硫酸锰(或MnSO4)
.




 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案