
 ��ͼ��ʾ��û��ͨ������������Ʊ�����ʱ��װ�ã�ͼ��a��b�ǿɿ��Ƶĵ������У�����֪�������ڱ����Ȼ�����Һ�е��ܽ�Ƚ�С��
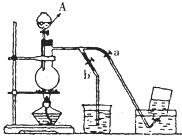
��ͼ��ʾ��û��ͨ������������Ʊ�����ʱ��װ�ã�ͼ��a��b�ǿɿ��Ƶĵ������У�����֪�������ڱ����Ȼ�����Һ�е��ܽ�Ƚ�С������ ��1���������ṹ��֪AΪ��Һ©��������Ũ������������̼����Ʊ���������Ӧ�����Ȼ��̡�������ˮ��
��2��������Һ�巽���ռ�������ˮ����Ϊ�����Ȼ�����Һ���ձ�����Һ���ն������������ֹ��Ⱦ������
��3����������HCl��������������Clԭ���غ���㱻����HCl�����ʵ�����
��� �⣺��1���������ṹ��֪AΪ��Һ©��������Ũ������������̼����Ʊ���������Ӧ�����Ȼ��̡�������ˮ����Ӧ����ʽΪ��MnO2+4HCl��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$MnCl2+Cl2��+2H2O��
�ʴ�Ϊ����Һ©����MnO2+4HCl��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$MnCl2+Cl2��+2H2O��
��2��������Һ�巽���ռ�������ˮ����Ϊ�����Ȼ�����Һ���ձ�����Һ���ն������������ֹ��Ⱦ���������ռ�����ʱ��Ӧ��a���ر�b���������ռ����ʱӦ��b���ر�a��
�ʴ�Ϊ����a���ر�b����b���ر�a��
��3����Ӧ��������Ϊ$\frac{0.672L}{22.4L/mol}$=0.03mol����������HCl��������������Clԭ���غ㣬������HCl�����ʵ���Ϊ0.03mol��2=0.06mol��
�ʴ�Ϊ��0.06mol��
���� ���⿼������ʵ�����Ʊ����漰��ѧ�������Ʊ�ԭ�����Բ�����װ�õķ������ۡ�������ԭ��Ӧ����ȣ��Ƚϻ�����ע��Ի���֪ʶ���������գ�


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

| ѡ�� | �� | �� | �� |
| A | �������ɫ���� | ��ʯ�� | ʪ�����ɫ���� |
| B | �������ɫ���� | �轺 | ʪ�����ɫ���� |
| C | ʪ�����ɫ���� | Ũ���� | �������ɫ���� |
| D | ʪ�����ɫ���� | ��ˮ�Ȼ��� | �������ɫ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��0.01mol•L-1Ba��OH��2��Һ�У�Na+��NH4+��NO3-��HCO3- | |
| B�� | ʹ���ȱ��ɫ����Һ�У�Mg2+��Fe2+��NO-3��Cl- | |
| C�� | ���б��ӵ���Һ�У�K+��Cl-��Br-��Fe3+ | |
| D�� | ˮ�����c��H+��=1��10-13mol•L-1����Һ�У�K+��Na+��I-��SO42- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | ��0.1mol-1•LNa2CO3��Һ��ͨ������CO2�����c��Na+��=2[c��HCO3-��+c��CO32-��+c��H${\;}_{{2}_{\;}}$CO3��] | |
| B�� | ��pH=8��NaB��Һ�У�c��Na+��-c��B-��=9.9��10-7mol•L-1 | |
| C�� | ��0.1mol•L-1NaHSO3��Һ��ͨ������NH3�����c��Na+��+c��H+��=c��HSO-3��+2c��SO32-�� | |
| D�� | ��0.1mol•L-1���Ȼ����Һ�У�c��Cl-����c��NH4+����c��H+����c��OH-�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | p��Ne����p��N2����p��O2�� | B�� | p��O2����p��Ne����p��N2�� | C�� | p��N2����p��O2����p��Ne�� | D�� | p��N2����p��Ne����p��O2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

| �������������������� ����۵� | ���ġ����ӷ���ʽ | |
| �� | ���е����ӷ���ʽ�����Ա�ʾһ�ѧ��Ӧ | 2Na+2H2O=2Na++2OH-+H2�� |
| �� | ��������кͷ�Ӧ���ɱ�ʾΪ H++OH-�TH2O | 2H++SO42-+Ba2++2OH-=BaSO4��+2H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ǿ��ʴ�� | |
| B�� | ��������������������ĸ��� | |
| C�� | ������������������ | |
| D�� | ����ʢ��Ũ������ձ��м�ˮϡ�ͳ�ϡ���� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com