
”¾ĢāÄæ”æ°Ń6molAĘųĢåŗĶ5molBĘųĢå»ģŗĻ·ÅČė4LĆܱÕČŻĘ÷ÖŠ£¬ŌŚŅ»¶ØĢõ¼žĻĀ·¢Éś·“Ó¦£ŗ
3A£ØĘų£©+B£ØĘų£© ![]() 2C£ØĘų£©+”£X D£ØĘų£©¾5min“ļµ½Ę½ŗā£¬“ĖŹ±Éś³ÉCĪŖ2mol £¬²ā¶ØDµÄĘ½¾ł·“Ó¦ĖŁĀŹĪŖ0.1mol/Lmin£¬ĻĀĮŠĖµ·ØÖŠ“ķĪóµÄŹĒ £Ø £©
2C£ØĘų£©+”£X D£ØĘų£©¾5min“ļµ½Ę½ŗā£¬“ĖŹ±Éś³ÉCĪŖ2mol £¬²ā¶ØDµÄĘ½¾ł·“Ó¦ĖŁĀŹĪŖ0.1mol/Lmin£¬ĻĀĮŠĖµ·ØÖŠ“ķĪóµÄŹĒ £Ø £©
A.x = 2
B. BµÄ×Ŗ»ÆĀŹĪŖ20%
C. Ę½ŗāŹ±AµÄÅضČĪŖ0.75mol/L
D. ŗćĪĀ“ļĘ½ŗāŹ±ČŻĘ÷ÄŚŃ¹ĒæĪŖæŖŹ¼Ź±µÄ85%
”¾“š°ø”æD
”¾½āĪö”æDµÄĘ½¾ł·“Ó¦ĖŁĀŹĪŖ0.1mol/Lmin£¬ŌņÉś³ÉDŹĒ0.1mol/Lmin”Į4L”Į5min£½2mol”£øł¾Ż±ä»ÆĮæÖ®±ČŹĒĻąÓ¦µÄ»Æѧ¼ĘĮæŹżÖ®±ČæÉÖŖ£¬x£½2£¬AÕżČ·”£øł¾Ż·½³ĢŹ½æÉÖŖ£¬ĻūŗÄAŗĶBµÄĪļÖŹµÄĮæ·Ö±šŹĒ3molŗĶ1mol£¬ĖłŅŌBµÄ×Ŗ»ÆĀŹŹĒ![]() £½20£„£¬BÕżČ·”£Ę½ŗāŹ±AµÄĪļÖŹµÄĮæŹĒ6mol£3mol£½3mol£¬ĘäÅØ¶ČŹĒ
£½20£„£¬BÕżČ·”£Ę½ŗāŹ±AµÄĪļÖŹµÄĮæŹĒ6mol£3mol£½3mol£¬ĘäÅØ¶ČŹĒ![]() £¬CÕżČ·”£·“Ó¦Ē°ŗóĢå»żŹĒ²»±äµÄ£¬Ņņ“ĖŃ¹ĒæŅ²ŹĒ²»±äµÄ£¬D²»ÕżČ·”£“š°øŃ”D”£
£¬CÕżČ·”£·“Ó¦Ē°ŗóĢå»żŹĒ²»±äµÄ£¬Ņņ“ĖŃ¹ĒæŅ²ŹĒ²»±äµÄ£¬D²»ÕżČ·”£“š°øŃ”D”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŠæĶŌµē³Ų×°ÖĆČēĶ¼ĖłŹ¾£¬ĘäÖŠŃōĄė×Ó½»»»Ä¤Ö»ŌŹŠķŃōĄė×ÓŗĶĖ®·Ö×ÓĶعż£¬ĻĀĮŠÓŠ¹ŲŠšŹöÕżČ·µÄŹĒ( )
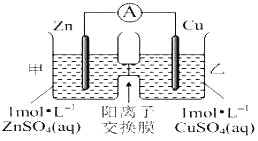
A. Ķµē¼«ÉĻ·¢ÉśŃõ»Æ·“Ó¦
B. µē³Ų¹¤×÷Ņ»¶ĪŹ±¼äŗ󣬼׳ŲµÄC(SO42-)¼õŠ”
C. µē³Ų¹¤×÷Ņ»¶ĪŹ±¼äŗó£¬ŅŅ³ŲČÜŅŗµÄ×ÜÖŹĮæŌö¼Ó
D. ŃōĄė×ÓĶعż½»»»Ä¤ĻņÕż¼«ŅĘ¶Æ£¬ŅõĄė×ÓĶعż½»»»Ä¤Ļņøŗ¼«ŅĘ¶Æ£¬±£³ÖČÜŅŗÖŠµēŗÉĘ½ŗā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠ·“Ó¦µÄĄė×Ó·½³ĢŹ½ÕżČ·µÄŹĒ£Ø £©
A.Ļņ·ŠĖ®ÖŠµĪ¼ÓFeCl3ČÜŅŗÖʱøFe£ØOH£©3½ŗĢå£ŗFe3++3H2O ![]() Fe£ØOH£©3”ż+3H+
Fe£ØOH£©3”ż+3H+
B.ÓĆŠ”ĖÕ“ņÖĪĮĘĪøĖį¹ż¶ą£ŗNaHCO3©+H+=Na++CO2”ü+H2O
C.ŹµŃéŹŅÓĆÅØŃĪĖįÓėMnO2·“Ó¦ÖĘCl2£ŗMnO2+4H++2Cl© ![]() Cl2”ü+Mn2++2H2O
Cl2ӟ+Mn2++2H2O
D.ÓĆFeCl3ČÜŅŗøÆŹ“Ó”Ė¢µēĀ·°å£ŗFe3++Cu=Fe2++Cu2+
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚ·“Ó¦£ŗC+CO2£½2COÖŠ£¬æÉŹ¹·“Ó¦ĖŁĀŹŌö“óµÄ“ėŹ©ŹĒ ( )
¢ŁŌö“óŃ¹Ēæ ¢ŚÉżøßĪĀ¶Č ¢ŪĶØČėCO2 ¢ÜŌö¼ÓĢ¼µÄĮæ ¢Ż½µµĶŃ¹Ēæ
A£®¢Ł¢Ś¢Ū B£®¢Ś¢Ū¢Ü¢Ż C£®¢Ł¢Ś¢Ū¢Ü D£®¢Ś¢Ū¢Ü
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”潫1molŅŅ“¼(ĘäÖŠµÄŃõÓĆ18O±ź¼Ē)ŌŚÅØĮņĖį“ęŌŚ²¢¼ÓČČĻĀÓė×ćĮæŅŅĖį³ä·Ö·“Ó¦£®ĻĀĮŠŠšŹöÕżČ·µÄŹĒ( )
A.Ė®·Ö×ÓÖŠŗ¬ÓŠ18OB.ŅŅĖįŅŅõ„ÖŠŗ¬ÓŠ18O
C.×īÖÕĢåĻµÖŠĖÄÖÖ·Ö×ÓÖŠ¶¼ŗ¬ÓŠ18OD.Éś³É90gŅŅĖįŅŅõ„
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĪ¢Į£¼äµÄ×÷ÓĆĮ¦ÖŠ£¬²»ŹōÓŚ»Æѧ¼üµÄŹĒ
A.·Ö×Ó¼ä×÷ÓĆĮ¦B.½šŹō¼üC.¹²¼Ū¼üD.Ąė×Ó¼ü
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĄė×Ó·½³ĢŹ½ÖŠ£¬ÕżČ·µÄŹĒ
A.FeʬĶ¶ČėÅØĮņĖįÖŠ£ŗFe+2H+”ś Fe2++H2”ü
B.ĮņĖįĀĮČÜŅŗµĪČė¹żĮæÉÕ¼īČÜŅŗÖŠ£ŗAl3++4OH£”ś AlO2£+ 2H2O
C.FeS·ÅČėĻ”ŃĪĖįČÜŅŗÖŠ£ŗS2£+2H+ ”śH2S”ü
D.ŌŚAlCl3ČÜŅŗÖŠ¼ÓČė¹żĮæ°±Ė®£ŗAl3++4NH3”¤H2O”ś AlO2£+4NH4++2H2O
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚŅ»ČŻ»żĪŖ2LµÄĆÜĶÅČŻĘ÷ÄŚ¼ÓČė0.2molN2ŗĶ0.6molH2£¬ŌŚŅ»¶ØĢõ¼žĻĀ·¢ÉśČēĻĀ·“Ó¦£ŗ ![]() N2(g)+
N2(g)+ ![]() H2(g)
H2(g)![]() NH3(g)
NH3(g)
¢ŁøĆ·“Ó¦µÄĘ½ŗā³£ŹżµÄ±ķ“ļŹ½ŹĒ:____________”£
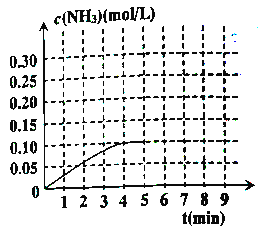
¢Ś·“Ó¦ÖŠ°±ĘųµÄÅØ¶ČµÄ±ä»ÆĒéæöČēĶ¼ĖłŹ¾£¬¼ĘĖć“Ó·“Ó¦æŖŹ¼µ½Ę½ŗāŹ±£¬Ę½¾ł·“Ó¦ĖŁĀŹv(H2)=________”£
¢ŪÅŠ¶ĻøĆ·“Ó¦“ļµ½Ę½ŗāדĢ¬µÄ±źÖ¾ŹĒ_________”£
a.N2ŗĶNH3ÅضČĻąµČ b.NH3°Ł·Öŗ¬Įæ±£³Ö²»±ä
c.ČŻĘ÷ÖŠĘųĢåµÄŃ¹Ēæ±£³Ö²»±ä d.NH3µÄÉś³ÉĖŁĀŹÓėH2µÄĻūŗÄĖŁĀŹĻąµČ
e.ČŻĘ÷ÖŠ»ģŗĻĘųĢåµÄĆܶȱ£³Ö²»±ä
¢Ü·“Ó¦“ļĘ½ŗāŗ󣬵Ś5·ÖÖÓÄ©£¬±£³ÖĘäĖüĢõ¼ž²»±ä£¬½öøı䷓ӦĪĀ¶Č£¬ŌņNH3µÄĪļÖŹµÄĮæÅØ¶Č²»æÉÄÜĪŖ______”£
a.0.2mol/L b.0.12mol/L c.0.10mol/L d.0.08mol/L
¢ŻŌŚµŚ5·ÖÖÓÄ©£¬½«ČŻĘ÷Ģå»żĖõŠ”Ņ»°ėŗó£¬ČōŌŚµŚ8·ÖÖÓÄ©“ļµ½ŠĀĘ½ŗā£Ø“ĖŹ±NH3ÅضČŌ¼ĪŖ0.25mol/L)£¬ĒėŌŚÉĻĶ¼ÖŠ»³ö“ÓµŚ5·ÖÖÓÄ©æŖŹ¼£¬ŌŁ“ļµ½ŠĀĘ½ŗāŹ±NH3ÅØ¶Č±ä»ÆĒśĻß”£______________
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĪļÖŹÖŠ£¬ŗ¬ÓŠ·Ē¼«ŠŌ¼üµÄĄė×Ó»ÆŗĻĪļŹĒ£Ø £©
A. Na2O2 B. Na2O C. NaOH D. CaCl2
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com