
| 离子 | 开始沉淀的pH | 沉淀完全的pH |
| Fe3+ | 1.0 | 3.0 |
| Fe2+ | 5.8 | 8.8 |
| Cu2+ | 4.2 | 6.7 |
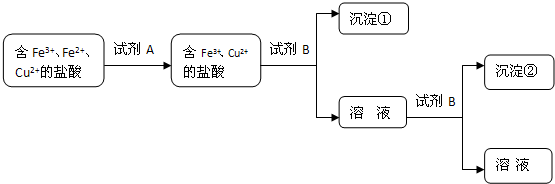


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、聚四氟乙烯分子中含有双键 |
| B、聚四氟乙烯的单体是不饱和烃 |
| C、聚四氟乙烯中氟的质量分数是76% |
| D、聚四氟乙烯的化学活性较大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
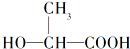 在一定条件下自身可发生缩聚反应,生成一种高聚物
在一定条件下自身可发生缩聚反应,生成一种高聚物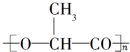 ,用这种新型高聚物制成的餐具,在乳酸菌的作用下,60天内可分解成无害的物质,不会对环境造成污染.在上述聚合反应中,生成的另一种产物是( )
,用这种新型高聚物制成的餐具,在乳酸菌的作用下,60天内可分解成无害的物质,不会对环境造成污染.在上述聚合反应中,生成的另一种产物是( )| A、CO2 |
| B、C2H5OH |
| C、H2O |
| D、CH3COOH |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、电解熔融AlCl3获取金属铝 |
| B、电解MgCl2溶液获取金属镁 |
| C、用CO还原铁矿石来获取金属铁 |
| D、电解饱和食盐水来获取金属钠 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、每生成16 mol N2转移30 mol电子 |
| B、NaN3中N元素被氧化 |
| C、N2既是氧化剂又是还原剂 |
| D、还原产物与氧化产物质量之比为1:15 |
查看答案和解析>>
科目:高中化学 来源: 题型:
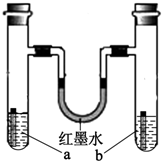 如图装置中,a、b试管内分别盛有食盐水和氯化铵溶液,各加入一块生铁片,放置一段时间.下列有关描述错误的是( )
如图装置中,a、b试管内分别盛有食盐水和氯化铵溶液,各加入一块生铁片,放置一段时间.下列有关描述错误的是( )| A、两块生铁片均发生电化学腐蚀 |
| B、墨水柱两边的液面变为左低右高 |
| C、两试管中相同的电极反应式为Fe-2e-=Fe2+ |
| D、a试管中发生了吸氧腐蚀,b试管中发生了析氢腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com