


 ��
�� ��
��
 ��
�� ���� �ɺϳ�ͼ��֪��A��B���������ϵĶ�λȡ����Ӧ����BΪ ��B��C����C=O�������ļӳɷ�Ӧ��C��D����-OH��-Clȡ����Ӧ����DΪ
��B��C����C=O�������ļӳɷ�Ӧ��C��D����-OH��-Clȡ����Ӧ����DΪ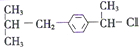 ������ϢR-Cl+NaCN��R-CN+NaCl��֪��D��E����ȡ����Ӧ��-Cl��-CNȡ������EΪ
������ϢR-Cl+NaCN��R-CN+NaCl��֪��D��E����ȡ����Ӧ��-Cl��-CNȡ������EΪ ��E������ҷ���ˮ������-COOH���ݴ˷������
��E������ҷ���ˮ������-COOH���ݴ˷������
��� �⣺�ɺϳ�ͼ��֪��A��B���������ϵĶ�λȡ����Ӧ����BΪ ��B��C����C=O�������ļӳɷ�Ӧ��C��D����-OH��-Clȡ����Ӧ����DΪ
��B��C����C=O�������ļӳɷ�Ӧ��C��D����-OH��-Clȡ����Ӧ����DΪ ������ϢR-Cl+NaCN��R-CN+NaCl��֪��D��E����ȡ����Ӧ��-Cl��-CNȡ������EΪ
������ϢR-Cl+NaCN��R-CN+NaCl��֪��D��E����ȡ����Ӧ��-Cl��-CNȡ������EΪ ��E������ҷ���ˮ������-COOH��
��E������ҷ���ˮ������-COOH��
��1��ͨ�����Ϸ���֪��B�ṹ��ʽΪ ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��
��2��A����ȡ����Ӧ����B��B�����ӳɷ�Ӧ����C��C����ȡ����Ӧ����D�����Է�Ӧ���ͷֱ���ȡ�����ӳɷ�Ӧ��ȡ����
�ʴ�Ϊ��ȡ�����ӳɣ�ȡ����
��3���л���C�뱽�Ӷ����б�����-OH����������-OH�뱽��ֱ�����������Ϊ�����廯����ʴ�Ϊ��D��
��4���� A ������ͬ�ķ���ʽ���ұ�����ֻ��һ��ȡ�������л��ﹲ�����֣����ݶ��������ֿ�֪����A�⣬������Ϊ ��
�� ��
�� ��
��
�ʴ�Ϊ�� ��
�� ��
�� ��
��
��5��E������ҷ�Ӧ�Ļ�ѧ����ʽΪ ��
��
�ʴ�Ϊ�� ��
��
���� ���⿼���л���ĺϳɣ���ȷ�ϳ��з�Ӧ������̼���Ǽܵı仯�������ŵı仯���ƶ������ǽ����Ĺؼ����ѵ���ͬ���칹��ṹ��ʽ��ȷ������Ŀ�Ѷ��еȣ�


 ����ѧ��Ӯ�����ϵ�д�
����ѧ��Ӯ�����ϵ�д� ѧ���쳵�����ּ��������ҵ�½����������ϵ�д�
ѧ���쳵�����ּ��������ҵ�½����������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| t/s | 0 | 500 | 1000 |
| c��N2O5��/mol•L-1 | 5.00 | 3.50 | 2.50 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
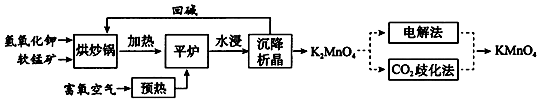
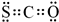
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���˲����У�������Ӧ��ʱ����©���� | |
| B�� | ����ʱ�����ܰ������������ʯ�����ϼ��� | |
| C�� | ��ȡ��Һʱ�������ϰ��ۻ�С��©����С�ף�Ȼ��������ܷų��²�Һ�� | |
| D�� | ��������ƿ������ʱ���ý�ͷ�ιܵμ�����ˮ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��״���£�22.4L���������������������ҷ�Ӧת�Ƶĵ�����Ϊ2NA | |
| B�� | ������1molFeCl3�ı�����Һ���뵽��ˮ�еõ������������壬���н������ӵ���ĿΪNA | |
| C�� | ����2.7g���ֱ���100 mLŨ��Ϊ2mol•L-1�����������������Һ��ַ�Ӧ��ת�Ƶĵ�������Ϊ0.3NA | |
| D�� | ͨ������£�16g CH4�к���4NA��C-H�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �Թ� | B�� | ������ | C�� | ���� | D�� | �ձ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ���� | NaCl | Na2CO3 | NaClO | NaHCO3 |
| pH | 7 | 11.6 | 9.7 | 8.3 |
| A�� | ����ͬ�¶��£�ͬŨ�ȵ���������Һ�ĵ���������HCl��H2CO3��HClO | |
| B�� | ����������ʵ���Ũ�ȵ�NaCl��Һ��NaClO��Һ��Cl-��ClO-���Ӹ�����Cl-��ClO- | |
| C�� | ��Na2CO3��Һ����ε�������ϡ���ᣬ��ӦΪ��Na2CO3+2HCl=2NaCl+CO2��+H2O | |
| D�� | ����CO2ͨ��0.1mol/L Na2CO3��Һ����Һ���ԣ�����Һ�У�2c��CO32-��+c��HCO3-��=0.2mol/L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ˮ������觡��챦ʯ������ʯ����Ҫ�ɷֶ��Ƿǽ��������� | |
| B�� | �������ǽṹ���ӵĸ߷��ӻ���������ʵ������������ȡ���ڵ����ʵ�һ���ṹ | |
| C�� | ͬλ��ʾ�ٷ����о���ѧ��Ӧ���̵��ֶ�֮һ����������������о��л�����ӽṹ���ζ����������ڲ�������������Һ��Ũ�� | |
| D�� | ��������������������Һ�뽺�壬�ơ�����ϡ������ܲ������������ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com