

| A、混合气体X一定含有SO2 |
| B、②中试剂可以是氨水或NaOH溶液 |
| C、③中操作为蒸发浓缩、冷却结晶 |
| D、①中硫酸的浓度一定为98% |


科目:高中化学 来源: 题型:
| A、氢氧化铜中加入盐酸 H++OH-=H2O |
| B、铁与盐酸反应 2Fe+6H+=2Fe3++3H2↑ |
| C、大理石与盐酸反应放出CO2气体:CO32-+2H+=CO2+H2O |
| D、氯化铁溶液中加入氢氧化钠溶液Fe3++3OH-=Fe(OH)3↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、各取少量于试管中加入几片铜片 |
| B、用玻璃棒各蘸少许点在滤纸上 |
| C、各取少量于试管中滴加NaOH溶液 |
| D、各取少量于试管中滴加BaCl2溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、甲苯既可使溴的四氯化碳溶液褪色,也可使酸性高锰酸钾溶液褪色 |
| B、有机物2-溴丁烷的消去产物有两种 |
| C、有机物A(C4H6O2)能发生加聚反应,可推知A的结构一定是CH2═CH-COOCH3 |
| D、可用溴水鉴别1-己烯、四氯化碳和乙酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na2O+H2O═2NaOH | ||||
| B、2F2+2H2O═4HF+O2 | ||||
| C、Cl2+H2O═HCl+HClO | ||||
D、3Fe+4H2O
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.1NA的NaHCO3 |
| B、0.05NA Na2CO3 |
| C、0.05NA~0.1NA Na2CO3和NaHCO3混合物 |
| D、0.1NA的NaHCO3和NaOH混合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、H2SO3是弱酸,所以Na2SO3是弱电解质 |
| B、SO3可以使品红、FeCl3溶液退色,分别体现了它的漂白性和还原性 |
| C、因为H2SO4溶液和Na2SO4溶液均具有良好的导电性,所以H2S04和Na2SO4均是离子化合物 |
| D、100mL 18.4mol?L-1的浓硫酸与足量铜在加热的条件下充分反应可产生9.2mol SO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
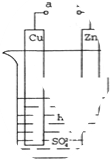 原电池是化学对人类的一项重大贡献.
原电池是化学对人类的一项重大贡献.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com