
| A、常温下,浓硫酸、浓硝酸均能将金属铜氧化,且均能使铁钝化 |
| B、乙烯常用作植物催熟剂,乙酸常用作调味剂,乙醇常用于杀菌消毒 |
| C、玛瑙、水晶、钻石的主要成分均为SiO2 |
| D、蛋白质、纤维素、蔗糖、天然橡胶都是高分子化合物 |


科目:高中化学 来源: 题型:
 甲、乙、丙、丁、戊是中学常见的无机物,其中甲、乙为单质,它们的转化关系如图所示(某些条件和部分产物已略去).下列说法不正确的是( )
甲、乙、丙、丁、戊是中学常见的无机物,其中甲、乙为单质,它们的转化关系如图所示(某些条件和部分产物已略去).下列说法不正确的是( )| A、若甲既能与盐酸反应又能与NaOH溶液反应,则丙可能属于两性氧化物 |
| B、若甲为短周期中原子半径最大的主族元素的单质,且戊为碱,则丙可能为Na2O2 |
| C、若甲、丙、戊含有同一种元素,则三种物质中,该元素的化合价由低到高的顺序一定为:甲<丙<戊 |
| D、若丙、丁混合产生白烟,且丙分子为18电子分子,丁分子为10电子分子,则乙的水溶液可能具有漂白作用 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、
| ||||||
| B、强电解质中不含共价键 | ||||||
| C、25℃时,pH=9的Na2CO3溶液和pH=5的AlCl3溶液中,水的电离程度相同 | ||||||
| D、25℃时,pH=4.75、浓度均为0.1mol?L-1的CH3COOH、CH3COONa的c(CH3COO-)+c(OH-)<c(CH3COOH)+c(H+)混合溶液: |
查看答案和解析>>
科目:高中化学 来源: 题型:
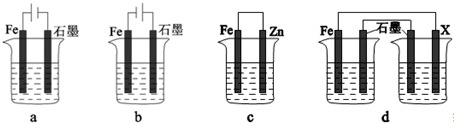
| Fe2O3 | CO | Fe | CO2 | |
| 甲/mol | 1.0 | 1.0 | 1.0 | 1.0 |
| 乙/mol | 1.0 | 2.0 | 1.0 | 1.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、聚乙烯食品包装袋、食物保鲜膜都是无毒的高分子化合物 |
| B、棉花、木材和羊毛的主要成分都是纤维素 |
| C、pH在5.6-7.0之间的降水通常称为酸雨 |
| D、汽油、植物油、甘油都有特殊的香味,都是酯类 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、乙醇和乙酸都能与金属钠反应,也都能发生酯化反应 |
| B、乙烯和苯都能使酸性KMnO4褪色,也都能发生加成反应 |
| C、乙酸和油脂都能与氢氧化钠溶液反应,也都能发生氧化反应 |
| D、淀粉和蛋白质都是天然高分子化合物,也都能发生水解反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
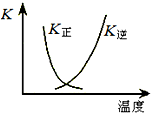 把a molO2和b mol SO2气体充入一密闭容器中,高温条件下发生反应O2+2SO2?2SO3
把a molO2和b mol SO2气体充入一密闭容器中,高温条件下发生反应O2+2SO2?2SO3| X |
| Y |
| 1 |
| 4 |
| X |
| Y |
| 2 |
| 3 |
| X |
| Y |
| 1 |
| 4 |
| X |
| Y |
| 3 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、N2H4(g)+2H2O2(l)═N2(g)+4H2O(g)△H=+817.63 kJ?mol-1 |
| B、N2H4(g)+2H2O2(l)═N2(g)+4H2O(g)△H=-641.63 kJ?mol-1 |
| C、N2H4(g)+2H2O2(l)═N2(g)+4H2O(g)△H=+641.63 kJ?mol-1 |
| D、N2H4(g)+2H2O2(l)═N2(g)+4H2O (g)△H=-817.63 kJ?mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 请回答下列问题.
请回答下列问题.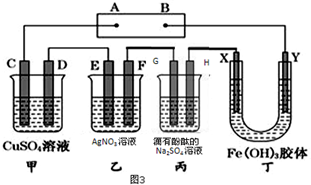
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com