
| �ܶ� ��g•mL-1�� | �۵� ���棩 | �е� ���棩 | �ܽ��� | |
| ������ | 1.2659 | 122.13 | 249 | ����ˮ���������Ҵ������ѵ��л��ܼ� |
| ���� | 1.07 | 40.6 | 181.9 | �������Ҵ������ѣ�65����������ˮ���� |
| �Ҵ� | 0.79 | -114.3 | 78.5 | ��ˮ���ܣ��ɻ������ѡ��ȷ¡����͵ȶ����� ���ܼ� |
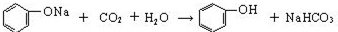 ��
��| ʵ�鲽�� | ����ͽ��� |
| ��ȡ�������Һ1���Թܣ��μ�BaCl2�� ������ | ������ɫ������BaCO3 |
| ��ȡ����������ϲ���ҹ���Թܣ��μ�0.1mol/L�����ٽ�����������ͨ�����ʯ��ˮ�� | ����ʯ��ˮ����� ˵�����Һ1����HCO3- |
| ����ȡ�������Һ1���Թܣ��μ�0.1mol/L FeCl3��Һ���� | ��Һ������ɫ�� ˵�����Һ1�����з��ǻ� |
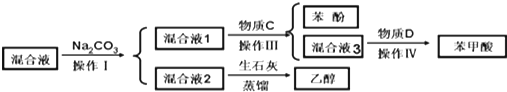
���� ��1����������ǿ����HCl�������H2CO3�����ӣ�HCO3-������ͱ��ӵ��Ҵ���Һ��̼���ƻ��ʱ����������̼���Ʒ�Ӧ�����ɱ������ơ�������̼��ˮ��������̼���Ʒ�Ӧ���ɱ����ƺ�̼�����ƣ����Ҵ���̼���ƶ�����Ӧ����ͼ�ɵã����Һ1����Ҫ�ɷ��DZ������ơ������ơ�̼�����ơ�̼���Ƶ����ʣ����Һ2����Ҫ�ɷ����Ҵ������ʣ���������ǿ��˳��������C��̼��������̼���壻
��������̼��������̼��ˮ�������ֽⷴӦ�����ɱ��ӡ�̼�����ƣ�������������̼��������̼��ˮ����Ӧ������Һ3����Ҫ�ɷ��DZ������ƺ�̼�����Ƶ����ʣ�����D�������HCl�������뱽�����Ʒ������ֽⷴӦ�����ɱ�������Ȼ��ƣ�������̼�����Ʒ������ֽⷴӦ�������Ȼ��ơ�������̼�����ˮ�����ڱ���������ˮ���������뱽�����Ʒ�Ӧ�����γɱ�����Ĺ�������Һʱ���������������ᾧ�壬����Һ�з���������ᾧ��IJ���IV�ǹ��ˣ�
��2�����Һ1�к��б����ƣ�ͨ�������̼���壬�۲쵽��Һ����ǣ���������H2CO3�����ӣ�HCO3-���ó�����Ϊ���Ӻ�̼�����ƣ�����д����ѧ��Ӧ����ʽ��
��3�����Һ2����Ҫ�ɷ�Ϊ�Ҵ���Ҫ�ռ��Ҵ���ͨ����ȡ����ķ�����������ʯ����ˮ��Ӧ�������ı仯�����д��⣻
��4�������1�к��б����ơ��������ơ�̼���ƣ�̼�����Ƶȣ���֤���б��Ӻ�̼�����ƣ����鱽�ӿɸ��ݱ������Ȼ�����ɫ��Ӧ�жϣ�����̼�����ƣ���Ҫ����̼���ƵĴ��ڣ��ų�̼���Ƶĸ��ţ��ٽ�̼�����ת��Ϊ������̼���м��飻
��5�����ݱ�״̬�¶�����̼��������ΪV=33.6mL�����Լ��������̼�����ʵ���n=$\frac{V}{Vm}$=$\frac{0.0336L}{22.4L/mol}$=0.0015mol���������������̼�����ʵ���֮��Ϊ1��1���������Ƶ�����m=n��M=0.0015mol��122g/mol�T0.183g����֪��Ʒ������m=2.0g��������������������������
��� �⣺��1�������ʷ��������ͼ����֪�����1�к��б����ƣ�Ҫ�Ƶñ��ӣ�����ǿ�������ᣨH2CO3�����ӣ���������Һ��ͨ��CO2���壬
���Һ3�к��б������ƣ�����D�������HCl�������뱽�����Ʒ�Ӧ���ɱ�������Ȼ��ƣ����ڱ���������ˮ���������뱽�����Ʒ�Ӧ�����γɱ�����Ĺ�������Һʱ���������������ᾧ�壬����IV�ǹ��ˣ�
�ʴ�Ϊ��CO2�����ˣ�
��2������ǿ��H2CO3�����ӣ�HCO3-������ǿ�������ᣬ��Ӧ����ʽΪ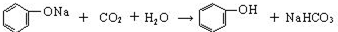 ��
��
�ʴ�Ϊ��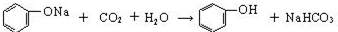 ��
��
��3�����Һ2�м�����ʯ�ҵ�ԭ������ʯ������Һ2�е�ˮ��Ӧ����������������Һ�������Ҵ��ӻ���������������
�ʴ�Ϊ����ʯ������Һ2�е�ˮ��Ӧ����������������Һ�������Ҵ��ӻ���������������
��4������̼���ƹ���������Һ1�п��ܺ��б������ơ������ơ�̼�����ơ�̼���Ƶ����ʣ�����̼�����ܸ���̼�����Ƶļ��飬��˲����Ӧ��ȡ�����ټ������0.1mol/L BaCl2�������ã���̼���������ȫ����Ϊ̼�ᱵ���ų�̼������Ӷ�̼��������ӵĸ��ţ����ݲ����������ͽ������ƣ�����̼�����������ǿ�������¿��Ա�Ϊ������̼���壬˵������ٵ��ϲ���Һ�еμ�����0.1mol/L���ᣬ�ٽ�����������ͨ�����ʯ��ˮ�У�����ʯ��ˮ����ǣ�˵����Һ1�к���̼��������ӣ����ڲ���2�м������������Խ�������ת��Ϊ���ӣ���˲������Ҫ��ȡ���Һ1�����ڱ������Ȼ�����Һ����ɫ�����������Ȼ�����Һ����ɫ��������Ũ��ˮ��Ӧ���ɰ�ɫ��������������Ũ��ˮ���ܲ�����ɫ�������������Ʒ�м���0.1mol/L FeCl3��Ũ��ˮ������Һ������ɫ�����ְ�ɫ�ij�������˵�����Һ1�����з��ǻ��ӣ���
| ʵ�鲽�� | ����ͽ��� |
| ��ȡһ�����������Թܣ���������0.1mol/L BaCl2 | ������ɫ������BaCO3 |
| ��ȡ����������ϲ���ҹ���Թܣ��μ������� 0.1mol/L���ᣬ�ٽ�����������ͨ�����ʯ��ˮ�� | ������������ҳ���ʯ��ˮ����ǣ�֤����HCO3- |
| ����ȡ�����������Թܣ��μ�����0.1mol/L FeCl3��Һ����������Ũ��ˮ������ | ��Һ������ɫ�����ְ�ɫ�ij����� |
| ʵ�鲽�� | ����ͽ��� |
| ��ȡһ�����������Թܣ���������0.1mol/L BaCl2 | ������ɫ������BaCO3 |
| ��ȡ����������ϲ���ҹ���Թܣ��μ������� 0.1mol/L���ᣬ�ٽ�����������ͨ�����ʯ��ˮ�� | ������������ҳ���ʯ��ˮ����ǣ�֤����HCO3- |
| ����ȡ�����������Թܣ��μ�����0.1mol/L FeCl3��Һ����������Ũ��ˮ������ | ��Һ������ɫ�����ְ�ɫ�ij����� |
���� ���⿼��̽��ʵ�鼰��ѧ���㣬�漰��������ͼ�����ֽⷴӦ�������Լ���ȷ��������������ᴿ�������ᴿ�ؼ�����Ļ�ѧ����ʽ�����ͳ����Լ������á����ʵ�鷽����ȥ̼�������л��е�̼���ơ����ʵ�鷽������̼�����ƵĴ��ڡ����ʵ�鷽�����鱽���Ƿ���ڡ��������������Ħ����������ʵ��������ʵ����ڻ�ѧ����ʽ�е�Ӧ�á�Ħ��������������������ʹ��ȼ��㡢��Ч���ֵĴ����ȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �л���ɷ��������������� | |
| B�� | ��C������������ | |
| C�� | �л��ﶼ������ˮ�����������л��ܼ� | |
| D�� | �л��ﶼ��ȼ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��
��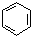 ��Ũ���������£���Ũ���ᷴӦ�Ļ�ѧ����ʽΪ
��Ũ���������£���Ũ���ᷴӦ�Ļ�ѧ����ʽΪ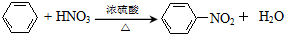 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢ڢۢ� | B�� | �� | C�� | �٢ڢ� | D�� | �٢ڢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
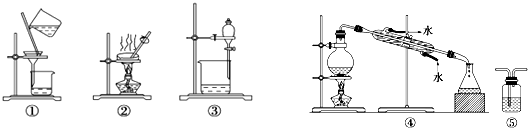
| A�� | ��CCl4��ȡ��ˮ�еĵ⣬ѡ�� | |
| B�� | ��KMnO4��Һ����CH4�Ƿ���C2H4��ѡ�� | |
| C�� | �����ᴿ��ѡ�ٺ͢� | |
| D�� | ʯ�͵ķ���ѡ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
| ʵ�鲽�� | ʵ������[ |
| �ٽ���������ˮ���뵽����NaBr��Һ�У��ٵ���������CCl4��Һ�������� | A����Һ��Ϊ�������㣬�ϲ�Ϊ��ɫ���²�Ϊ�Ⱥ�ɫ |
| �ڽ���������ˮ���뵽����KI��Һ�У��ٵ���������CCl4��Һ�������� | B����Һ��Ϊ�������㣬�ϲ�Ϊ��ɫ���²�Ϊ�Ϻ�ɫ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | һ���м��� | B�� | һ������ϩ | ||
| C�� | һ��û������ | D�� | �����Ǽ������ϩ�Ļ���� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com