
| A. | 2molSO2+1molO2 | B. | 2molSO2+1molO2+2molSO3 | ||
| C. | 4molSO2+1molO2 | D. | 3molSO2+0.5molO2+1molSO3 |
分析 在一定条件下,将2mol SO2和2mol SO3气体充入固定体积的密闭容器,发生反应,2SO2+O2?2SO3可以看做与起始量为4mol SO2,1molO2 反应达到平衡是相同的平衡状态,各物质的浓度不变,物质的量不变,SO3为nmol;
A、起始充入2molSO2和1molO2,相当于在原平衡基础上减少了2molSO2,减少反应物二氧化硫的量,平衡逆向进行,消耗三氧化硫;
B、起始充入2molSO2和1molO2和2molSO3,相当于起始加入了4molSO2和2molO2,可看做在原平衡的基础上加入1molO2,平衡正向移动,三氧化硫增加;
C、起始充入4molSO2和1molO2正好与原平衡相同;
D、起始充入3molSO2+0.5molO2+1molSO3,相当于起始加入了4molSO2和1molO2,正好与原平衡相同.
解答 解:A、起始量和题给起始量相比,相当于减少2molSO2,减少反应物二氧化硫的量,平衡逆向进行,三氧化硫物质的量<n,故A不选;
B、起始量相当于加入4molSO2和2molO2,可看做在原平衡的基础上加入1molO2,平衡正向移动,三氧化硫物质的量>nmol,故B选;
C、起始量与题给起始量相同,平衡相同,SO3物质的量为n mol,故C不选;
D、起始充入3molSO2+0.5molO2+1molSO3,相当于起始加入了4molSO2和1molO2,正好与原平衡相同,平衡相同,SO3物质的量为n mol,故D不选;
故选B.
点评 本题考查了可逆反应,要注意用化学平衡中的等效平衡的判断方法,明确极限转化后起始量的大小是解答的关键.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 加入FeCl3固体 | B. | 加水 | C. | 加入少量浓盐酸 | D. | 升温 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3CH2 CH2CH3和 CH3CH(CH3)2 | |
| B. | CH3CH2 CH2COOH 和 HOOCCH2CH2CH2CH3 | |
| C. | CH3CH2OH 和CH3OCH3 | |
| D. | CH2=C(CH3)2和CH3CH=CHCH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 17gNH3所含中子数目为10 NA | |
| B. | 常温常压下,22 g氧气和26 g臭氧所含的氧原子总数为3NA | |
| C. | 常温常压下,18g H2O含有的电子总数为8NA | |
| D. | 常温常压下,2.24LCO和CO2混合气体中含有的碳原子数目为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,500mL 2mol•L-1的Na2CO3溶液中含Na+数目为NA | |
| B. | 常温下,2.7g铝与足量盐酸反应,失去电子数为0.3NA | |
| C. | 1.8gNH4+的离子中含有的质子数为0.1NA | |
| D. | 标准状况下,1 L水所含分子数为$\frac{1}{22.4}$NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na---Na2O2---Na2CO3---NaHCO3 | B. | Fe---Fe3O4---FeCl2---Fe(OH)3 | ||
| C. | Si---SiO2---H2SiO3---Na2SiO3 | D. | S---SO2---SO3--H2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
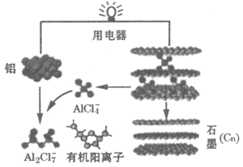 2015年斯坦福大学研究人员研制出一种可在一分钟内完成充放电的超常性能铝离子电池,内部用AlCl4-和有机阳离子构成电解质溶液,其放电工作原理如图所示.下列说法不正确的是( )
2015年斯坦福大学研究人员研制出一种可在一分钟内完成充放电的超常性能铝离子电池,内部用AlCl4-和有机阳离子构成电解质溶液,其放电工作原理如图所示.下列说法不正确的是( )| A. | 放电时,铝为负极、石墨为正极 | |
| B. | 放电时,有机阳离子向铝电极方向移动 | |
| C. | 放电时的负极反应为:Al-3e-+7AlCl4-═4Al2Cl7- | |
| D. | 充电时,AlCl4-向石墨电极方向移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com