
���� ��1����������İ�ˮ���Ȳ����裬Mg2+��Fe2+��Fe3+ ��Al3+�����ɳ������������������ӣ���Fe��OH��2�ױ���������Fe��OH��3�����˺�����������ᣬ������Һ�к���Mg2+��Fe3+ ��Al3+��
��2��Na2O2��ˮ��Ӧ�����������ƣ���Һ�ʼ��ԣ�Na2O2����ǿ�����ԣ�����OH-��Ӧ�����Ӻ;��л�ԭ�Ե����ӵ�Ũ�Ȼᷢ���ı䣬ͬʱ��Һ�д��ڷ�Ӧ���ɵ����ӣ�������Ũ��Ҳ��仯��
��� �⣺��1����������İ�ˮ���Ȳ����裬Mg2+��Fe2+��Fe3+ ��Al3+�����ɳ������������������ӣ���Fe��OH��2�ױ���������Fe��OH��3�����˺�����������ᣬ������Һ�к���Mg2+��Fe3+ ��Al3+���������Ϊ���ʴ�Ϊ��Mg2+��Al3+��
��2��Na2O2��ˮ��Ӧ�����������ƣ���Һ�ʼ��ԣ�OH-��Na+Ũ������
HCO3-��OH-��Ӧ����CO32-����HCO3-����Ũ�ȼ�С��CO32-����Ũ������
Na2O2����ǿ�����ԣ���SO32-����ΪSO42-����SO32-����Ũ�ȼ�С��
NH4+��OH-��Ӧ��NH4+Ũ�ȼ�С��
CH3COO-Ũ�Ȼ������䣮
�ʴ�Ϊ��CH3COO-��
���� ���⿼�����ӵĹ��棬Ϊ��Ƶ���㣬����ϰ���е���Ϣ����������֮��ķ�ӦΪ���Ĺؼ������ظ��ֽⷴӦ�Ŀ��飬ע������������������ԭ��Ӧ�������м����ᣬ��Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
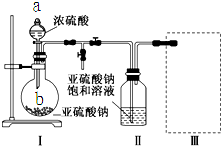 ���������ƣ�Na2S2O5���dz��õ�ʳƷ��������֮һ��ij�о�С���������ʵ�飺
���������ƣ�Na2S2O5���dz��õ�ʳƷ��������֮һ��ij�о�С���������ʵ�飺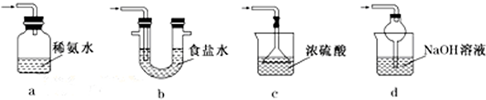
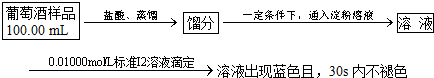
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ���� | �����Լ� | ȥ���ᴿ���� |
| �����ʣ�NaCl�� | ||
| ���������ͣ� |
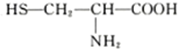 ����ˮ�����γɶ��ĵĽṹ��ʽΪ��
����ˮ�����γɶ��ĵĽṹ��ʽΪ��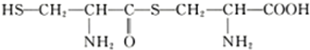 ��
�� +3NaOH $\stackrel{����}{��}$3C17H35COONa+
+3NaOH $\stackrel{����}{��}$3C17H35COONa+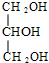 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

 ������뽫Br2��Na2CO3��Ӧ�Ļ�ѧ����ʽ��������
������뽫Br2��Na2CO3��Ӧ�Ļ�ѧ����ʽ���������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1��1 | B�� | 1��3 | C�� | 1��4 | D�� | 2��3 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com