
下列物质的分离方法不正确的是( )
|
| A. | 用过滤的方法除去食盐中泥沙 |
|
| B. | 用蒸馏的方法将自来水制成蒸馏水 |
|
| C. | 用酒精萃取碘水中的碘 |
|
| D. | 用水冲洗的方法从沙里淘金 |
考点:
物质的分离、提纯的基本方法选择与应用.
专题:
实验题.
分析:
A.泥沙不溶于水,食盐溶于水;
B.自来水中含有盐类物质,利用沸点不同制取蒸馏水;
C.酒精和水互溶;
D.根据金的密度较大来分析.
解答:
解:A.泥沙不溶于水,食盐溶于水,则能用过滤的方法除去食盐中泥沙,故A正确;
B.自来水中含有盐类物质,利用沸点不同制取蒸馏水,则一般用蒸馏的方法将自来水制成蒸馏水,故B正确;
C.酒精和水互溶,则不能用酒精萃取碘水中的碘,一般选择苯或四氯化碳作萃取剂,故C错误;
D.因金的密度较大,则能用水冲洗的方法从沙里淘金,故D正确;
故选C.
点评:
本题考查物质的分离、提纯方法的选择,注意物质的性质差异选择合理的分离方法是解答本题的关键,选项B为解答的易错点,题目难度不大.


 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案科目:高中化学 来源: 题型:
在石灰窑中烧制生石灰,1 mol CaCO3完全分解所需要的能量,可燃烧0.453 mol碳来提供。设空气中O2体积分数为0.21,N2为0.79,则石灰窑产生的气体中CO2的体积分数可能是( )
A.0.43 B.0.46 C.0.49 D..0.52
查看答案和解析>>
科目:高中化学 来源: 题型:
黄铁矿(主要成分为FeS2)是工业制取硫酸的重要原料,其煅烧产物为SO2和Fe3O4。
(1)将0.050molSO2(g)和0.030molO2(g)放入容积为1L的密闭容器中,反应:2SO2(g)+O2(g) 2SO3(g)在一定条件下达到平衡,测得c(SO3)=0.040mol/L。计算该条件下反应的平衡常数K和SO2的平衡转化率(写出计算过程)。
2SO3(g)在一定条件下达到平衡,测得c(SO3)=0.040mol/L。计算该条件下反应的平衡常数K和SO2的平衡转化率(写出计算过程)。
(2)已知上述反应是放热反应,当该反应处于平衡状态时,在体积不变的条件下,下列措施中有利于提高SO2平衡转化率的有 (填字母)
A 升高温度 B 降低温度 C 增大压强
D 减小压强 E 加入催化剂 G 移出氧气
(3)SO2尾气用饱和Na2SO3溶液吸收可得到重要的化工原料,反应的化学方程式为
。
(4)将黄铁矿的煅烧产物Fe3O4溶于H2SO4后,加入铁粉,可制备FeSO4。酸溶过程中需保持溶液足够酸性,其原因是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
有X、Y、Z三种元素,已知:
①X2-、Y-均与Y的气态氢化物分子具有相同的电子数;
②Z与Y可组成化合物ZY3,ZY3溶液遇苯酚呈紫色。
请回答:
(1)Y的最高价氧化物对应水化物的化学式是______________。
(2)将ZY3溶液滴入沸水可得到红褐色液体,反应的离子方程式是___________________,此液体具有的性质是______(填写序号字母)。
a.光束通过该液体时形成光亮的“通路”
b.插入电极通直流电后,有一极附近液体颜色加深
c.向该液体中加入硝酸银溶液,无沉淀产生
d.将该液体加热、蒸干、灼烧后,有氧化物生成
(3)X单质在空气中燃烧生成一种无色有刺激性气味的气体。
①已知一定条件下,每1 mol该气体被O2氧化放热98.0 kJ。若2 mol该气体与1 mol O2在此条件下发生反应,达到平衡时放出的热量是176.4 kJ,则该气体的转化率为________。
②原无色有刺激性气味的气体与含1.5 mol Y的一种含氧酸(该酸的某盐常用于实验室制取氧气)的溶液在一定条件下反应,可生成一种强酸和一种氧化物,若有1.5×6.02×1023个电子转移时,该反应的化学方程式是_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:4NH3+5O2 4NO+6H2O 4NO+3O2+2H2O→4HNO3
4NO+6H2O 4NO+3O2+2H2O→4HNO3
设空气中氧气的体积分数为0.20,氮气体积分数为0.80,请完成下列填空及计算
(1)a mol NO完全转化为HNO3需要氧气_______ mol
(2)为使NH3恰好完全氧化为一氧化氮,氨-空气混合物中氨的体积分数为________(保留2位小数)。
(3)20.0 moL的NH3用空气氧化,产生混合物的组成为:NO 18.0 mol、O2 12.0 mol、N2 150.0 mol和一定量的硝酸,以及其它成分。(高温下NO和O2不反应)计算氨转化为NO和HNO3的转化率。
(4)20.0 moL 的NH3和一定量空气充分反应后,再转化为HNO3
①在下图中画出HNO3的物质的量n(A)和空气的物质的量n(B)关系的理论曲线。
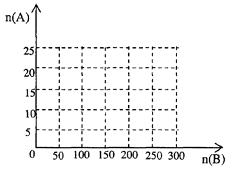
②写出当125≤n(B)≤200时,n(A)和n(B)的关系式______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
|
| A. | 1mol任何气体所含分子数都相同,体积也都约为22.4 L |
|
| B. | 1molKClO3和1molSO2中,所含氧原子的个数比为3:2 |
|
| C. | 物质的量就是物质的摩尔质量 |
|
| D. | 在非标准状况下,1 mol任何物质的体积都不是22.4 L |
查看答案和解析>>
科目:高中化学 来源: 题型:
在无色透明强酸性溶液中,能大量共存的离子组是( )
|
| A. | K+、Cu2+、NO3﹣、SO42﹣ | B. | K+、Na+、Cl﹣、CO32﹣ |
|
| C. | Zn2+、NH4+、NO3﹣、Cl﹣ | D. | K+、Na+、MnO4﹣、SO42﹣ |
查看答案和解析>>
科目:高中化学 来源: 题型:
为验证淀粉水解可生成还原性糖,进行了下列实验,该实验中操作步骤的排列顺序正确的是( )
①取少量淀粉加水制成溶液; ②加热煮沸; ③加入新制的Cu(OH)2悬浊液; ④加入几滴稀H2SO4;⑤加热; ⑥加入碱液中和并呈碱性.
|
| A. | ①④⑤⑥③② | B. | ⑤④②③①⑥ | C. | ①④②③⑤⑥ | D. | ①⑤③④⑥② |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com