
【题目】按要求完成下列问题:
(1)甲基的电子式_________________
(2)电石气的结构式_______________
(3)相对分子质量为72且沸点最低的烷烃的结构简式____________
(4)聚2﹣丁烯的结构简式___________________________
(5)与H2加成生成2,5﹣二甲基己烷的炔烃的系统命名_________________
(6)![]() 的系统命名__________________________
的系统命名__________________________
【答案】![]() H—C≡C—H
H—C≡C—H 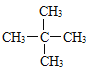
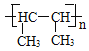 2,5﹣二甲基-3-己炔 4-甲基-2-乙基-1-戊烯
2,5﹣二甲基-3-己炔 4-甲基-2-乙基-1-戊烯
【解析】
(1)C原子与3个H原子结合形成甲基;
(2)乙炔气体俗称电石气,在乙炔中两个C原子形成3对共用电子对,每个C原子与1个H原子形成1个共用电子对;
(3)根据烷烃的分子式通式CnH2n+2,先结合其相对分子质量确定分子式,然后利用同分异构体中支链越多,沸点越低,书写结构简式;
(4)2-丁烯结构简式是CH3-CH=CH-CH3,2-丁烯发生加聚反应产生聚2-丁烯;
(5)根据炔烃与氢气发生加成反应时,碳链结构不变,两个不饱和的C原子上分别添加2个H原子得到相应的烷烃,然后进行逆推,就可得原来的炔烃,然后进行命名;
(6)选择含有碳碳双键在内的最长的碳链为主链,从离双键较近的一端给主链碳原子编号,以确定双键和支链的位置进行命名。
(1)C原子与3个H原子结合形成甲基,剩余甲基的电子式为:![]() ;
;
(2)电石的主要成分是CaC2,CaC2与水反应产生的乙炔气体俗称电石气,在乙炔中两个C原子形成3对共用电子对,每个C原子再与1个H原子形成1个共用电子对,剩余乙炔的电子式为:![]() ,结构式是H—C≡C—H;
,结构式是H—C≡C—H;
(3)烷烃的分子式通式CnH2n+2,相对分子质量14n+2=72,解得n=5所以分子式为C5H12,有CH3CH2CH2CH2CH3、![]() 、
、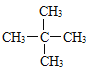 三种不同结构,由于同分异构体中,物质含有的支链越多,沸点越低,因此沸点最低的物质的结构简式为
三种不同结构,由于同分异构体中,物质含有的支链越多,沸点越低,因此沸点最低的物质的结构简式为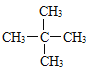 ;
;
(4)2-丁烯结构简式是CH3-CH=CH-CH3,2-丁烯发生加聚反应产生聚2-丁烯,其结构简式是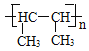 ;
;
(5)由于炔烃与氢气发生完全加成反应时,不饱和的碳碳叁键中断开较不稳定的两个键,然后这2个C原子分别结合2个H原子变为饱和C原子。由于炔烃加成反应产生是2,5﹣二甲基己烷,逆推可知原来的炔烃的结构为![]() ,名称为2,5﹣二甲基-3-己炔;
,名称为2,5﹣二甲基-3-己炔;
(6)选择含有碳碳双键在内的最长的碳链为主链,从离双键较近的一端给主链碳原子编号,以确定双键和支链的位置进行命名,该物质的名称为4-甲基-2-乙基-1-戊烯;


 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案 导学教程高中新课标系列答案
导学教程高中新课标系列答案科目:高中化学 来源: 题型:
【题目】一种肼燃料电池的结构如图所示,下列说法正确的是( )
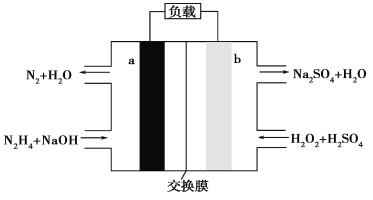
A. a极是正极,电极反应式为N2H4-4e-+4OH-=N2↑+4H2O
B. 电路中每转移NA个电子,就有1mol Na+穿过膜向正极移动
C. b极的电极反应式为H2O2+2e-=2OH-
D. 用该电池作电源电解饱和食盐水,当得到0.1mol Cl2时,至少要消耗0.1mol N2H4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为实验室某浓硫酸试剂瓶标签上的相关数据,据此回答有关问题:

(1)该浓硫酸物质的量浓度为________________。
(2)取用任意体积的该浓硫酸时,下列物理量中不随所取体积的多少而变化的是_________(填字母序号)。
a.溶液中H2SO4的物质的量 b.溶液的浓度 c.溶液的密度
(3)某同学欲用上述浓硫酸和蒸馏水配制500mL0.400mol·L﹣1的稀硫酸。提供的仪器有:胶头滴管、玻璃棒、烧杯、量筒、细口试剂瓶。
①配制稀硫酸时,还缺少的仪器有_______________(写名称),该仪器上标有_____(填字母序号)。
a.温度 b.浓度 c.容量 d.压强 e.刻度线
②该学生需要量取_________mL上述浓硫酸进行配制。
③在配制过程中,下列实验操作对所配制得稀硫酸的物质的量浓度有何影响? (在横线上填写“偏大”、“偏小”或“无影响”)用量筒量取浓硫酸时俯视观察凹液面__________________;定容、摇匀后静置,液面低于刻度线,继续加水至刻度线________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)有下列几组物质,请将序号填入下列空格内:
A.CH2=CH-COOH和油酸(C17H33COOH) B.12C60和石墨
C.![]() 和
和 ![]() D.35Cl和37Cl E.乙醇和乙二醇
D.35Cl和37Cl E.乙醇和乙二醇
①互为同位素的是_____________; ②互为同系物的是________________;
③互为同素异形体的是__________;④互为同分异构体的是_____________;
⑤既不是同系物,又不是同分异体,也不是同素异形体,但可看成是同一类物质的是____。
(2)写出下列有机物的系统命名或结构简式:
A.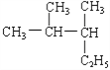 :________________________;
:________________________;
B.CH3CH(CH3)C(CH3)2(CH2)2CH3:_______________________;
C.3,4-二甲基-4-乙基庚烷:______________________________;
D.2-甲基-2-丁烯:_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】冬日,雪花漫舞,银装素裹,给人们带来美的享受,但降雪却会给道路通行带来麻烦。现有一种高速公路的绿色融雪剂——CMA(醋酸钙、醋酸镁固体混合物),其生产常以白云石(主要成分MgCO3·CaCO3,含SiO2等杂质)和生物质废液——木醋液(主要成分乙酸,以及少量的甲醇、苯酚、焦油等杂质)等为原料,流程如图:
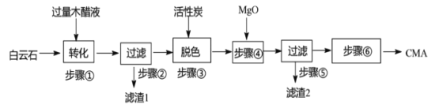
(1)步骤①发生的反应离子方程式为____。
(2)滤渣1的主要成分与NaOH溶液反应的热化学方程式为___(己知与l mol NaOH发生反应时放出热量为QkJ)。步骤②所得滤液常呈褐色,分析可知其原因主要是木醋液中含有少量的有色的焦油以及____。
(3)已知CMA中钙、镁的物质的量之比与出水率(与融雪效果成正比)关系如图所示,步骤④的目的除调节n(Ca)∶n(Mg)约为__(选填:A.1∶3;B.1∶2;C.3∶7;D.2∶3)外,另一目的是___。
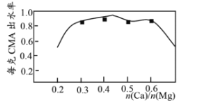
(4)步骤⑥包含的操作有___、过滤、洗涤及干燥。
(5)取akg含MgCO3·CaCO3质量分数为b%的白云石,经过上述流程制备CMA。已知MgCO3·CaCO3的损失率为c%,步骤④之后到产品CMA的损失率为d%,则结合(3)可知所得产品质量约为____kg(请用含相关字母的计算式表达,不必化简)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在标准状况下有:①6.72LCH4,②3.01×1023个HCl分子,③13.6gH2S,④0.2molNH3。下列对这四种气体的描述正确的是( )
a. 体积②>③>①>④ b. 密度②>③>④>①
c. 质量②>③>①>④ d. 氢原子个数①>③>④>②
A. abc B. bcd C. abd D. abcd
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学—选修5 有机化学基础】某抗结肠炎药物有效成分的合成路线如下(部分反应略去试剂和条件):
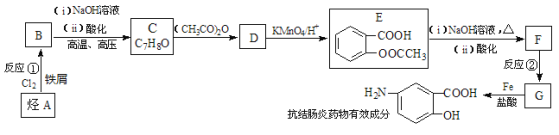
已知:
请回答下列问题:
(1)抗结肠炎药物有效成分的分子式是:_____________;烃A的名称为:_____________;反应②的反应类型是:___________________。
(2)①下列对该抗结肠炎药物有效成分可能具有的性质推测正确的是:____________;
A.水溶性比苯酚好 B.能发生消去反应也能发生聚合反应
C.1mol该物质最多可与4mol H2发生反应 D.既有酸性又有碱性
② E与足量NaOH溶液反应的化学方程式是:_______________________。
(3)符合下列条件的抗结肠炎药物有效成分的同分异构体有________种。
A.遇FeCl3溶液有显色反应 B.分子中甲基与苯环直接相连 C.苯环上共有三个取代基
(4)已知:苯环上连有烷基时再引入一个取代基,常取代在烷基的邻对位,而当苯环上连有羧基时则取代在间位,据此按先后顺序写出以A为原料合成邻氨基苯甲酸(![]() )合成路线中两种中间产物的结构简式(部分反应条件已略去)
)合成路线中两种中间产物的结构简式(部分反应条件已略去)
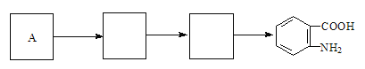
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关![]() 反应的叙述正确的为
反应的叙述正确的为
A.还原剂与氧化剂物质的量之比为5:3
B.生成lmolO2,反应共转移4mol电子
C.若有5mol水做还原剂时,被BrF3还原的BrF3为![]() mol
mol
D.若有5mol水参与反应时,被水还原的BrF3为2mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空:
(1)有相同温度和压强下的两种气体12C18O和14N2,若两种气体的质量相同,则两种气体所含的质子数之比为__________,若两种气体的原子数相等,则两种气体所含中子数之比_________,若两种气体的体积相同,则两种气体的密度之比为_________。
(2)10.8 g R2O5中氧原子的数目为3.01×1023,则元素R的相对原子质量为 ________。
(3)将10 mL1.00 mol/L Na2CO3溶液与10 mL1.00 mol/L CaCl2溶液相混和,则混和溶液中Na+的物质的量浓度为___________(忽略混合前后溶液体积的变化)。
(4)在标准状况下,由CO和CO2组成的混合气体为6.72 L,质量为12 g,此混合物中CO和CO2物质的量之比是_________。
(5)在空气中煅烧CoC2O4生成钴的氧化物和CO2,测得充分煅烧后固体质量为2.41g,CO2的体积为1.344L(标准状况),则钴氧化物的化学式为_______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com