
 ������ĩ��ϰ��ѵ��ϵ�д�
������ĩ��ϰ��ѵ��ϵ�д� С��ʿ��ĩ����100��ϵ�д�
С��ʿ��ĩ����100��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
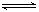 SO3(g)����H����98.32 kJ/mol���������г���2 mol SO2��1 mol O2��ַ�Ӧ�����շų�������Ϊ
SO3(g)����H����98.32 kJ/mol���������г���2 mol SO2��1 mol O2��ַ�Ӧ�����շų�������Ϊ| A��196.64 kJ | B��196.64 kJ/mol | C����196.64 kJ | D����196.64 kJ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
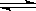 2C(g) һ��ʱ���ﵽƽ�⣬����amolC��������˵������ȷ���ǣ�
2C(g) һ��ʱ���ﵽƽ�⣬����amolC��������˵������ȷ���ǣ�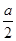 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
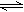 2Z��g������H>0����Ϊ��������Z�����ɣ�Ӧ���õķ�Ӧ�����ǣ� ��
2Z��g������H>0����Ϊ��������Z�����ɣ�Ӧ���õķ�Ӧ�����ǣ� ��| A�����¸�ѹ | B�����µ�ѹ | C�����¸�ѹ | D�����µ�ѹ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2AB��g���ﵽƽ��״̬�ı�־�ǣ� ��
2AB��g���ﵽƽ��״̬�ı�־�ǣ� ��| A���������ܵ�ѹǿ����ʱ��仯 |
| B�������ڵ������ʵ�������ʱ��仯 |
| C����λʱ��������2n mol AB��ͬʱ����n mol B2 |
| D��������A2��B2��AB�����ʵ���֮����1��1��2ʱ��״̬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�������
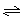 xC(g)��2D(g)����5 min���D��Ũ��Ϊ0.5 mol/L��c(A)��c(B)��3��5��C��ƽ����Ӧ����Ϊ0.1 mol/(L��min)����
xC(g)��2D(g)����5 min���D��Ũ��Ϊ0.5 mol/L��c(A)��c(B)��3��5��C��ƽ����Ӧ����Ϊ0.1 mol/(L��min)�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������

�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com