
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
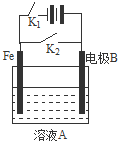 根据图示装置,下列说法不正确的是( )
根据图示装置,下列说法不正确的是( )| 选项 | 开关状态 | 溶液A | 电极B | 说明 |
| A | 打开K1,闭合K2 | NaCl | 石墨 | 正极反应:O2+2H2O+4e-=4OH- |
| B | 打开K1,闭合K2 | NaCl | Zn | 铁制品保护:牺牲阳极的阴极保护法 |
| C | 打开K2,闭合K1 | CuSO4 | Cu | 铁表面镀铜 |
| D | 打开K2,闭合K1 | CuSO4 | 粗铜 | 电解法精炼铜 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温常压下4.6g NO2和N2O4混合气体所含原子总数为0.3NA |
| B、标准状况下,22.4L SO3的分子数为NA |
| C、1molFe在22.4L的Cl2(标准状况下)燃烧,转移的电子总数为3NA |
| D、电解58.5 g熔融的NaCl,能产生22.4 L氯气(标准状况)、23.0 g金属钠 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、该化合物仅含碳、氢两种元素 |
| B、该化合物中碳、氢原子个数比为1:2 |
| C、无法确定该化合物是否含有氧元素 |
| D、该化合物中一定含有氧元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
A、
| ||
B、
| ||
C、
| ||
D、
|
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
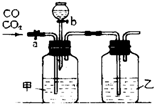 某学生用如图装置进行一氧化碳和二氧化碳混合气体的分离提纯及干燥.其中a为弹簧夹,b为分液漏斗的活塞.
某学生用如图装置进行一氧化碳和二氧化碳混合气体的分离提纯及干燥.其中a为弹簧夹,b为分液漏斗的活塞.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com