
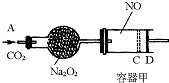
 如图装置中,容器甲内充入0.1mol NO气体,干燥管内装有一定量Na2O2,从A处缓慢通入CO2气体.恒温下,容器甲中活塞缓慢由D向左移动,当移至C处时容器体积缩小至最小,为原体积的
如图装置中,容器甲内充入0.1mol NO气体,干燥管内装有一定量Na2O2,从A处缓慢通入CO2气体.恒温下,容器甲中活塞缓慢由D向左移动,当移至C处时容器体积缩小至最小,为原体积的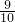 ,随着CO2的继续通入,活塞又逐渐向右移动.(不考虑活塞的磨擦)
,随着CO2的继续通入,活塞又逐渐向右移动.(不考虑活塞的磨擦)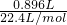 =0.04mol,
=0.04mol,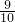 )=0.01mol
)=0.01mol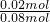 ×100%=25%,
×100%=25%,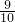 )
)

 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
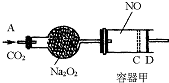 (2006?揭阳二模)如图装置中,容器甲内充入0.1mol NO气体,干燥管内装有一定量Na2O2,从A处缓慢通入CO2气体.恒温下,容器甲中活塞缓慢由D向左移动,当移至C处时容器体积缩小至最小,为原体积的
(2006?揭阳二模)如图装置中,容器甲内充入0.1mol NO气体,干燥管内装有一定量Na2O2,从A处缓慢通入CO2气体.恒温下,容器甲中活塞缓慢由D向左移动,当移至C处时容器体积缩小至最小,为原体积的| 9 | 10 |
查看答案和解析>>
科目:高中化学 来源: 题型:
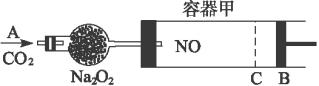
(1)①已知当活塞移至C处时,干燥管中物质的质量增加了2.24 g。此时,通入标准状况下的CO2气体多少升?容器甲中NO2转化为N2O4的转化率是多少?
②活塞移至C处后,继续通入a mol CO2,此时活塞恰好回至B处,则a值必小于0.01。其理由是_______________________________________________________。
(2)若改变干燥管中Na2O2的量,可通过调节甲容器的温度及通入CO2的量,使活塞发生从B到C,又从C到B的移动。则Na2O2的质量最小值应大于______________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
如图装置中,容器甲内充入0.1 mol NO气体,干燥管内装有一定量Na2O2,从A处缓缓通入CO2气体。恒温下,容器甲中活塞缓慢由B向左移动,当移至C处时,容器体积缩小至最小,为原体积的![]() 。随着CO2的继续通入,活塞又逐渐向右移动。
。随着CO2的继续通入,活塞又逐渐向右移动。
![]()
(1)①已知当活塞移至C处时,干燥管中物质的质量增加了2.24 g。此时,通入标准状况下的CO2气体多少升?容器甲中NO2转化为N2O4的转化率是多少?
②活塞移至C处后,继续通入a mol CO2,此时活塞恰好回至B处,则a值必小于0.01。其理由是_________________________________________________________________________。
(2)若改变干燥管中Na2O2的量,可通过调节甲容器的温度及通入CO2的量,使活塞发生从B到C,又从C到B的移动。则Na2O2的质量最小值应大于______________g。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年上海市徐汇区高三上学期期末教学质量调研(一模)化学试卷(解析版) 题型:计算题
如图装置中,容器甲内充入0.1
mol NO气体,干燥管内装有一定量Na2O2,从A处缓慢通入CO2气体.恒温下,容器甲中活塞缓慢由D向左移动,当移至C处时容器体积缩小至最小,为原体积的 ,随着CO2的继续通入,活塞又逐渐向右移动。(不考虑活塞的磨擦)
,随着CO2的继续通入,活塞又逐渐向右移动。(不考虑活塞的磨擦)

已知: 2Na2O2 + 2CO2 → 2Na2CO3 + O2
(1)已知当活塞移至C处时,干燥管中物质的质量增加了2.24 g。
①此时,通入标准状况下的CO2气体多少L?
②容器甲中NO2转化为N2O4的转化率是多少?
③活塞移至C处后,继续通入a mol CO2,此时活塞恰好回至D处.则a值必 0.01(填大于、小于、等于),其理由是 。
(2)若改变干燥管中Na2O2的量,要通过调节甲容器的温度及通入的量CO2,使活塞发生从D到C,又从C到D的移动,则Na2O2的质量最小值应大于________g。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com