
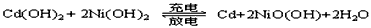
科目:高中化学 来源: 题型:
 CH3OH
CH3OH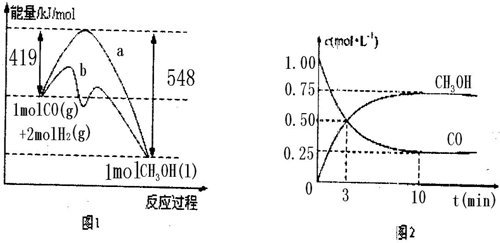
| 3 |
| 2 |
| 3 |
| 2 |
 CH3OH(g)△H<0的平衡常数为
CH3OH(g)△H<0的平衡常数为| 1 |
| 2 |
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 工业上常利用CO和H2合成可再生能源甲醇.
工业上常利用CO和H2合成可再生能源甲醇.查看答案和解析>>
科目:高中化学 来源:2013-2014学年河南省洛阳市高三上学期期末质量检测化学试卷(A卷)(解析版) 题型:填空题
工业上常利用CO和H2合成可再生能源甲醇。
(1)已知CO(g)、CH3OH(l)的燃烧热分别为283.0 kJ·mol-1和726.5 kJ·mol-1,则CH3OH(l)不完全燃烧生成CO(g)和H2O(l)的热化学方程式为 。
(2)合成甲醇的方程式为CO(g)+2H2(g) CH3OH(g) ΔH <0。
CH3OH(g) ΔH <0。
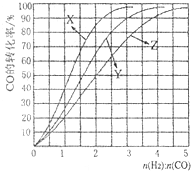
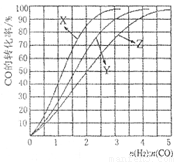
在230 ℃〜270 ℃最为有利。为研究合成气最合适的起始组成比n(H2):n(CO),分别在230 ℃、250 ℃和270 ℃进行实验,结果如下左图所示。其中270 ℃的实验结果所对应的曲线是_____(填字母);当曲线X、Y、Z对应的投料比达到相同的CO平衡转化率时,对应的反应温度与投较比的关系是 。
(3)当投料比为1∶1,温度为230 ℃,平衡混合气体中,CH3OH的物质的量分数为 (保留1位小数);平衡时CO的转化率 。
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)、已知①CO(g) + 1/2 O2(g) =CO2(g) ΔH1= -283.0 kJ/mol
②H2(g) + 1/2 O2(g) = H2O(l) ΔH2= -285.8 kJ/mol
③C2H5OH(l) + 3O2(g) = 2CO2 (g) + 3H2O(l) ΔH3=-1370 kJ/mol
试计算④2CO(g)+ 4H2(g)= H2O(l)+C2H5OH(l) 的ΔH4 ?
(2)、镍镉(Ni-Cd)可充电电池在现代生活中有广泛应用,镍镉可充电电池中的电解质溶液为KOH溶液,Cd(OH)2、Ni(OH)2、NiO(OH)都难溶于KOH溶液。它的充放电反应按下式进行:
![]()
请分别写出该电池在放电及充电时的电极反应式。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com