
【题目】某学习小组利用反应 制取
制取![]() 溶液的实验装置如图所示(已知:
溶液的实验装置如图所示(已知: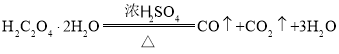 )下列说法正确的是( )
)下列说法正确的是( )
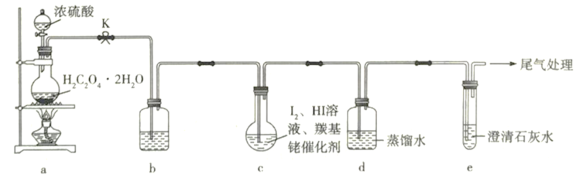
A.装置b中可盛放足量的浓![]() 溶液
溶液
B.装置c合适的加热方式是热水浴
C.反应后取少量装置c中溶液并滴加![]() 溶液,有黄色沉淀生成,说明
溶液,有黄色沉淀生成,说明![]() 被还原
被还原
D.若装置e中溶液未见浑浊,说明该实验条件下一定没有![]() 生成
生成
科目:高中化学 来源: 题型:
【题目】下列关于苯的叙述正确的是( )
A.苯与溴水混合振荡,二者发生加成反应,静置后溴水层为无色
B.由苯的结构式![]() 可知,苯分子中含C=C键,能使溴的四氯化碳溶液褪色
可知,苯分子中含C=C键,能使溴的四氯化碳溶液褪色
C.由苯的分子式C6H6可知,苯是不饱和烃,能与溴水发生加成反应
D.苯不能使酸性高锰酸钾溶液褪色,说明苯分子中不含碳碳双键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机物说法不正确的是
A. 命名为2-乙基-1,3-二丁烯
命名为2-乙基-1,3-二丁烯
B.沸点比较:乙二醇>乙醇>乙烷
C.含8个碳原子的有机物的分子中可能形成8个C—C单键
D. 属于芳香烃且属于苯的同系物
属于芳香烃且属于苯的同系物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】表示溶液中浓度的方法通常有两种:溶液中溶质的质量分数(w)和物质的量浓度(c),因此在配制溶液时,根据不同的需要,有不同的配制方法,请完成填空。
(1)用10%(密度为1.01 g·cm-3)的氢氧化钠溶液配制成27.5 g 2% 的氢氧化钠溶液。
①计算:需________g 10%(密度为1.01 g·cm3)的氢氧化钠溶液,其体积为________mL,需加________mL水(ρ水=1 g·cm-3)进行稀释。
②量取:用________mL量筒取10% 氢氧化钠,量取时视线要跟量筒________保持水平,然后倒入烧杯里,用________mL量筒量取蒸馏水也注入烧杯里。
③溶解:用________将上述溶液搅拌均匀,即得27.5 g 2% 的氢氧化钠溶液。
(2)用98%(密度为1.84 g·cm-3)的浓硫酸稀释成3 mol·L-1的稀硫酸100 mL,回答下列问题:
①需要取浓硫酸________mL;
②配制操作可分解成如下几步,以下正确的操作顺序是__________________________(填字母,下同)。
A.向容量瓶中注入少量蒸馏水,检查是否漏水
B.用少量蒸馏水洗涤烧杯及玻璃棒,将溶液注入容量瓶,并重复操作两次
C.用已冷却的稀硫酸注入已检查不漏水的容量瓶中
D.根据计算,用量筒量取一定体积的浓硫酸
E.将浓硫酸沿烧杯壁慢慢注入盛有蒸馏水的小烧杯中,并不断用玻璃棒搅拌
F.盖上容量瓶塞子,振荡,摇匀
G.用胶头滴管滴加蒸馏水,使溶液凹面恰好与刻度线相切
H.继续往容量瓶中小心地加蒸馏水,使液面接近刻度线
(3)实验室需配制1 mol·L-1的氢氧化钠溶液和1 mol·L-1的硫酸溶液各100mL。
①要配制氢氧化钠溶液,在用托盘天平称取氢氧化钠固体时,天平读数为________。
A.4.0 g B.4.00 g C.>4.0 g
②在配制氢氧化钠溶液和硫酸溶液的各步操作中,有明显不同的是__________。
A.称量或量取 B.溶解或稀释 C.移液、洗涤 D.定容
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用真空碳热还原冶炼镁、铝及锰的单质或合金是治金工业的热点之一。回答下列问题:
(1)已知体系自由能变化![]() 时反应能自发进行。
时反应能自发进行。![]() 真空碳热还原冶炼镁的主要反应为
真空碳热还原冶炼镁的主要反应为![]() ,其自由能变化与温度、压强的关系如图所示:
,其自由能变化与温度、压强的关系如图所示:

温度由低到高的顺序是_______________,![]() 时该反应不能自发进行的温度是_________(填“
时该反应不能自发进行的温度是_________(填“![]() ”“
”“![]() ”或“
”或“![]() ”)。
”)。
(2)![]() 提出的碳热还原
提出的碳热还原![]() 冶炼
冶炼![]() 的机理如下:
的机理如下:
(Ⅰ)![]()
(Ⅱ)![]()
(Ⅲ)![]()
则反应![]() 的
的![]() ______________
______________![]() (用含a、b、c的代数式表示);中间体之一
(用含a、b、c的代数式表示);中间体之一![]() 与
与![]() 反应可用于实验室制备甲烷,写出
反应可用于实验室制备甲烷,写出![]() 与
与![]() 反应的化学方程式:_________________________________________________________。
反应的化学方程式:_________________________________________________________。
(3)制备锰合金的相关反应及平衡时![]() 与温度的关系如图所示(
与温度的关系如图所示(![]() 为用分压表示的平衡常数,分压=总压×体积分数):
为用分压表示的平衡常数,分压=总压×体积分数):
(Ⅰ)![]()
(Ⅱ)![]()
(Ⅲ)![]()
①![]() 的反应是___________(填标号)。
的反应是___________(填标号)。
②![]() ____________[用
____________[用![]() 、
、![]() 表示];A点
表示];A点![]() ___________用[
___________用[![]() 表示]。
表示]。
③向某恒容密闭容器中充入![]() 并加入足量
并加入足量![]() ,若只发生反应:
,若只发生反应:![]() ,达到B点的平衡状态。达到平衡前,v(正)__________v(逆)(填“大于”“小于”或“等于”),达到平衡时,
,达到B点的平衡状态。达到平衡前,v(正)__________v(逆)(填“大于”“小于”或“等于”),达到平衡时,![]() _______________(保留小数点后两位)。
_______________(保留小数点后两位)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丙烯是重要的化工原料,以丙烯为原料合成有机玻璃和油墨材料DAP-A树脂的流程如下:

回答问题:
(1)写出下列物质可能的结构简式:B___________________,F________________________。
(2)写出反应类型:反应②___________________;反应③____________________________。
(3)1 mol DAP-A树脂在一定条件下与H2发生加成反应,最多消耗H2_______________mol。
(4)写出反应①的化学方程式_____________________________________________________。
(5)写出G在一定条件下与乙二醇发生反应生成一种高分子化合物的化学方程式为_______。
(6)E的同分异构体中,属于酯类的链状有机物有HCOOCH2CH=CH2、HCOOCH=CHCH3、___________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】烟气中SO2和NOx(NO及NO2)的脱除对于环境保护意义重大。
(1)湿式氨法烟气脱硫脱氮是通过氨水吸收烟气,得到含![]() 、
、![]() 、
、![]() 、
、![]() 和NO2的吸收液。
和NO2的吸收液。
①用离子方程式解释吸收液中含有![]() 的原因:_____________;
的原因:_____________;
②吸收液中的![]() 、
、![]() 均对NO2具有吸收作用,但
均对NO2具有吸收作用,但![]() 对NO2的吸收能力比
对NO2的吸收能力比![]() 弱,
弱,![]() 与NO2反应生成
与NO2反应生成![]() 的离子方程式是:___________;
的离子方程式是:___________;
(2)经测定,在烟气的吸收过程中,吸收液对NO2的吸收率随烟气通入量变化的曲线如下图所示。

结合化学用语解释产生上述结果的原因:_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如下图所示,△H1=-393.5 kJmol-1,△H2=-395.4 kJmol-1,下列说法或表示式正确的是( )

A. C(s、石墨)==C(s、金刚石)△H=+1.9kJmol-1
B. 石墨和金刚石的转化是物理变化
C. 金刚石的稳定性强于石墨
D. 1 mol石墨的总键能比1 mol金刚石的总键能小1.9 kJ
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com