
| A. | 原子半径:Z>Y>X | |
| B. | CaX2、CaY2和CaZ2等3种化合物中,阳离子与阴离子个数比均为1:2 | |
| C. | CaY2与水发生氧化还原反应时,CaY2只作氧化剂 | |
| D. | Z与X形成化合物的沸点高于Z的同族元素与X形成化合物的沸点 |
分析 X、Y、Z是原子序数依次递增的短周期元素,3种元素的原子核外电子数之和与Ca2+的核外电子数相等,即三元素原子核外电子数之和为18,Z得到1个电子变成8电子结构,则Z为F元素,X、Y一定至少有一种位于第2周期,X得到一个电子后均形成稀有气体原子的稳定电子层结构,故X为H元素,Y元素原子核外电子数为18-1-9=8,故Y为O元素,据此解答.
解答 解:X、Y、Z是原子序数依次递增的短周期元素,3种元素的原子核外电子数之和与Ca2+的核外电子数相等,即三元素原子核外电子数之和为18,Z得到1个电子变成8电子结构,则Z为F元素,X、Y一定至少有一种位于第2周期,X得到一个电子后均形成稀有气体原子的稳定电子层结构,故X为H元素,Y元素原子核外电子数为18-1-9=8,故Y为O元素.
A.原子半径应为Y(O)>Z(F)>X(H),故A错误;
B.CaO2其阴离子为O22-,阴、阳离子个数比为1:1,故B错误;
C.CaO2与水发生反应时,CaO2中O元素化合价由-1降低为-2价、由-1价升高为0价,既是氧化剂又是还原剂,故C错误;
D.HF分子之间含有氢键,沸点高于其它同族氢化物的沸点,故D正确,
故选:D.
点评 本题考查结构性质位置关系、氧化还原反应等,难度中等,推断元素是解题关键,C选项中根据过氧化钠的性质进行解答.


科目:高中化学 来源: 题型:选择题
| A. | ①③④ | B. | ②③ | C. | ①②③ | D. | ①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酸能使紫色石蕊试液变红,二氧化碳也能使紫色石蕊变红,所以二氧化碳是酸 | |
| B. | 某物质在空气中燃烧后生成二氧化碳和水,则该物质中一定含有氧元素 | |
| C. | 向某溶液中滴加氯化钡溶液,产生不溶于稀硝酸的白色沉淀,说明该溶液中可能存在SO42- | |
| D. | 溶液中有晶体析出,其溶质的质量减少,所以溶质的质量分数一定减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

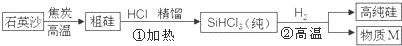
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | $\frac{8M}{{N}_{A}•{a}^{3}}$ | B. | $\frac{6M}{{N}_{A}•{a}^{3}}$ | C. | $\frac{4M}{{N}_{A}•{a}^{3}}$ | D. | $\frac{M}{{N}_{A}•{a}^{3}}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 物质 | 密度/(g•mL-1) | 沸点 | 水溶性 | 溶解性 |
| 甲 | 0.893 | 78.5℃ | 溶 | 溶于乙 |
| 乙 | 1.220 | 100.7℃ | 溶 | 溶于甲 |
| A. | 蒸馏 | B. | 升华 | C. | 分液 | D. | 过滤 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 7:1 | B. | 7:2 | C. | 7:3 | D. | 7:4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com