
 可用于补钙抗过敏等,以工业碳酸钙(含少量Na+、Al3+、Fe3+等杂质)生产医用二水合氯化钙(CaCl2 ·2H2O的质量分数为97.3—103.0%),工艺流程为:
可用于补钙抗过敏等,以工业碳酸钙(含少量Na+、Al3+、Fe3+等杂质)生产医用二水合氯化钙(CaCl2 ·2H2O的质量分数为97.3—103.0%),工艺流程为: 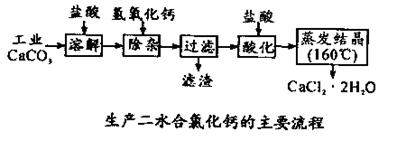

 结晶要保持在160℃: 。
结晶要保持在160℃: 。 。
。科目:高中化学 来源:不详 题型:填空题

 出行
出行查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.某山区发现了一种“柴油树”,它产生的树油可替代柴油使用 |
| B.新型材料碳纳米管的化学性质常温下很稳定 |
| C.美国最新研制出一种燃料电池,其能量转化率很高,可达到100% |
| D.蜘蛛丝(主要成分是蛋白质分子)强度特别大,可以用来制造防弹衣和降落伞绳 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Br2是氧化产物 | B.氯气是还原剂 |
| C.氯气是氧化剂 | D.该反应属于复分解反应 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.热分解法、热还原法、电解法 | B.热还原法、热分解法、电解法 |
| C.电解法、热还原法、热分解法 | D.电解法、热分解法、热还原法 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
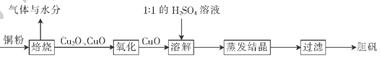
| A.加人稀H2SO4,若溶液呈蓝色,说明固体中一定有CuO |
| B.加人稀H2SO4,若有红色沉淀物生成,说明固体中一定有Cu2O |
| C.加人稀HNO3,若有无色气体(随即变成红棕色:)产生,说明固体中有Cu2O |
| D.加人稀HNO3,若固体全部溶解,说明固体中没有Cu2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com