
| A、溶液中溶质是Na2CO3和NaOH |
| B、溶液中的离子浓度:c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+) |
| C、溶液中的离子浓度:c(Na+)>c(HCO3-)=c(CO32-)>c(OH-)>c(H+) |
| D、溶液中的离子浓度:c(Na+)>c(CO32-)>c(HCO3-)>c(OH-)>c(H+) |
| n(NaOH) |
| n(CO2) |
| 3 |
| 2 |
|
| n(NaOH) |
| n(CO2) |
| 3 |
| 2 |
|


科目:高中化学 来源: 题型:
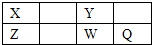 短周期元素X、Y、Z、W、Q在元素周期表的位置如表所示,其中X元素的原子内层电子数是最外层电子数的一半,则下列说法不正确的是( )
短周期元素X、Y、Z、W、Q在元素周期表的位置如表所示,其中X元素的原子内层电子数是最外层电子数的一半,则下列说法不正确的是( )| A、钠与W可能形成Na2W2化合物 |
| B、由X与Q两种元素组成的物质在熔融时不能导电 |
| C、X和Z的单质均有原子晶体 |
| D、X有多种同素异形体,而Y不存在同素异形体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Zn|H2SO4(稀)|Fe |
| B、Cu|AgNO3(aq)|Ag |
| C、Zn|CCl4|Cu |
| D、Fe|H2SO4(稀)|C |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、28g氮气所含有的原子数目为NA |
| B、标准状况下,22.4LH2O含有的分子数为 NA |
| C、NA 个CO2分子占有的体积一定为22.4L |
| D、标准状况下,22.4L H2和O2混合气所含的分子数一定等于NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2,2-二甲基丁烷的一氯代物有3种 |
| B、乙烯与苯都存在碳碳双键 |
| C、可用酸性KMnO4溶液鉴别苯、甲苯、己烯与四氯化碳 |
| D、等物质的量的乙烯与乙醇完全燃烧时,其耗氧量不相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 4 |
| 7 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:



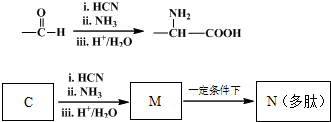
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com