
 A+B+C
A+B+C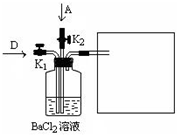 ______.
______. A+B+C,且A为刺激性气体,C为无色无味气体,应为氯碱工业的重要反应,甲为NaCl溶液,A为Cl2,B为NaOH,C为H2;
A+B+C,且A为刺激性气体,C为无色无味气体,应为氯碱工业的重要反应,甲为NaCl溶液,A为Cl2,B为NaOH,C为H2;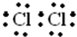 ,故答案为:
,故答案为: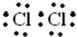 ;
;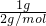 =0.5mol,在Cl2中燃烧时放出92.3kJ的热量,则1molH2反应放出的热量为184.6kJ,反应的热化学方程式为H2(g)+Cl2(g)=2HCl(g);△H=-184.6kJ/mol,
=0.5mol,在Cl2中燃烧时放出92.3kJ的热量,则1molH2反应放出的热量为184.6kJ,反应的热化学方程式为H2(g)+Cl2(g)=2HCl(g);△H=-184.6kJ/mol, ,故答案为:Cl2 +SO2+BaCl2+2H2O=BaSO4↓+4HCl;
,故答案为:Cl2 +SO2+BaCl2+2H2O=BaSO4↓+4HCl; ;
;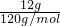 =0.1mol,反应过程中转移1.5mol电子,则1molFeS2转移15mol电子,则Fe被氧化为+3价,S被氧化为+6价,反应的离子方程式为FeS2 +14H++15NO3-=Fe3++2SO42-+15 NO2↑+7H2O,
=0.1mol,反应过程中转移1.5mol电子,则1molFeS2转移15mol电子,则Fe被氧化为+3价,S被氧化为+6价,反应的离子方程式为FeS2 +14H++15NO3-=Fe3++2SO42-+15 NO2↑+7H2O, A+B+C,且A为刺激性气体,C为无色无味气体,应为氯碱工业的重要反应,甲为NaCl溶液,A为Cl2,B为NaOH,C为H2;
A+B+C,且A为刺激性气体,C为无色无味气体,应为氯碱工业的重要反应,甲为NaCl溶液,A为Cl2,B为NaOH,C为H2;

 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
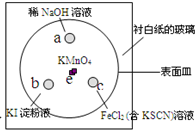 (2011?崇明县一模)如图,化学实验的微型化可有效减少污染,实现化学实验的绿色要求.某学生在一块衬白纸的玻璃片的不同位置分别加一滴含酚酞的NaOH溶液(a)、浓度为0.1mol/L KI淀粉溶液(b)、FeCl2(含KSCN)溶液(c),并在e处放置少量KMnO4晶体,向KMnO4晶体上滴加几滴浓盐酸后立即用表面皿盖好,形成一个气室.
(2011?崇明县一模)如图,化学实验的微型化可有效减少污染,实现化学实验的绿色要求.某学生在一块衬白纸的玻璃片的不同位置分别加一滴含酚酞的NaOH溶液(a)、浓度为0.1mol/L KI淀粉溶液(b)、FeCl2(含KSCN)溶液(c),并在e处放置少量KMnO4晶体,向KMnO4晶体上滴加几滴浓盐酸后立即用表面皿盖好,形成一个气室.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 已知 | 类比推理 |
| A | Na与O2共热生成Na2O2 | H2与O2共热生成H2O2 |
| B | S、Se属于VIA族元素 | Se的氧化物类似S有SeO2、SeO3 |
| C | 常温下,浓硝酸使铁钝化 | 浓硝酸与铜不反应 |
| D | NaOH溶液能溶解Al(OH)3 | 过量NH3?H2O缓慢溶解Al(OH)3 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com