
| ||
| ||
| H2SO4 |
| CuO |
| H2SO4 |
| Fe |
| ||
| ||
| ||


 �¿α�ͬ��ѵ��ϵ�д�
�¿α�ͬ��ѵ��ϵ�д� һ����ʦ����Ӧ����������һ��ȫϵ�д�
һ����ʦ����Ӧ����������һ��ȫϵ�д� Сѧѧϰ�ð���ϵ�д�
Сѧѧϰ�ð���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�




�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�������£�ͭ���������ѷ�Ӧ����Ϊͭ�������ķ�Ӧ�����ȷ�Ӧ |
| B��������ڳ��ºͼ����������������Ӧ�IJ��ﲻͬ |
| C����ɫ��Ӧʵ���еIJ�˿Ӧ��ϡ����ϴ�� |
| D�������ڿ����������ۻ����������䣬˵����������û�з�����ѧ��Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�����³�ѹ��11.2LN2���еķ�����Ϊ0.5N0 |
| B��9mLˮ�ͱ�״����11.2L����������ͬ�ķ�������עˮ���ܶ�Ϊ1g/mL�� |
| C��ͬ��ͬѹ�£�N0��NO��N0��N2��02�Ļ������������� |
| D��25�桢1.01��105Paʱ��11.2L����������ԭ����ĿΪN0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
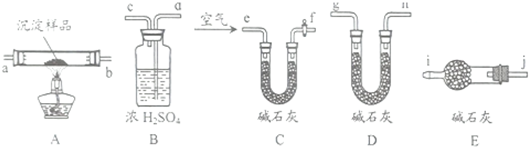
| ʵ�鲽�� | Ԥ������ | ���� |
| �ٳ���B��D�������ֱ�Ϊml��m2����װ�ð� f��a��b�� | ||
| �ڳ�ȡһ�������ij��� | ��1����m1=m3��m2��m4 ��2����m1 m2 ��3����ml m2 | ��1������1���� ��2������2���� ��3������3���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�����M��Һ��ǿ���ԣ���N��Һ�п��ܺ��е��������У�OH-��NO3-��CO32- |
| B�����M��Һ��ǿ���ԣ���N��Һ�п��ܺ��е��������У�MnO4-��AlO2-��SO42- |
| C�����M��Һ����ǿ��ԭ�ԣ���N��Һ�п��ܺ��е��������У�MnO4-��NO3-��SO42- |
| D�����M��Һ����ǿ�����ԣ���N��Һ�п��ܺ��е��������У�K+��Na+��NH4+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
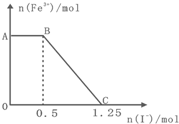 ��֪���Ը��������Һ���Խ�FeSO4��������ѧ��Ӧ����ʽΪ��
��֪���Ը��������Һ���Խ�FeSO4��������ѧ��Ӧ����ʽΪ��| A��ͼ��AB����Ҫ�Ǹ�����غ͵⻯����Һ��Ӧ | ||||
| B��ͼ��BC�η����ķ�ӦΪ2Fe3++2I-�T2Fe2++I2ͨ�� | ||||
| C������OC�ε����ݿ�֪��ʼ����ĸ�����ص����ʵ���Ϊ0.25mol | ||||
D����PtΪ�缫���ϵ��C�����Һ���ܷ�ӦʽΪ2H2O
|
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com