
已知短周期元素甲、乙、丙、丁、戊的原子序数依次增大,它们的部分化合价如下表。下列说法正确的是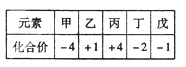
| A.乙的单质中能与水剧烈反应 |
| B.气态氢化物的稳定性:丙>甲 |
| C.丙的氧化物能与戊的氢化物水溶液反应 |
| D.其最高价氧化物对应的水化物的酸性:丁>戊 |
 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案科目:高中化学 来源: 题型:单选题
下列各组物质的性质比较中,正确的是
| A.热稳定性:H2O>HF>H2S | B.沸点:HF>HCl>HBr |
| C.密度:CH3CH2CH2Cl>CH3CH2Cl>CH3Cl | D.氧化性:Fe3+>Cu2+>H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
元素周期表和元素周期律可以指导人们进行规律性的推测和判断。下列说法不合理的是( )
| A.若X+和Y2-的核外电子层结构相同,则原子序数:X>Y |
| B.由水溶液的酸性:HCl>H2S,可推断出元素的非金属性:Cl>S |
| C.在元素周期表中,硅、锗都位于金属与非金属的交界处,都可以作半导体材料 |
| D.Cs和Ba分别位于第六周期ⅠA族和ⅡA族,碱性:CsOH>Ba(OH)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
X、Y、Z、W是元素周期表中原子序数依次增大的四种短周期元素,其相关信息如下表:
| 元素 | 相关信息 |
| X | 啤酒和饮料中常溶有X的最高价氧化物,打开瓶子时,这种氧化物会大量逸出 |
| Y | Y2是空气中含量最高的气体单质 |
| Z | Z的基态原子最外层电子排布式为2s22p4 |
| W | W的一种核素质量数为27,中子数为14 |
 Y2O4(g) △H2=-56.9kJ/mol
Y2O4(g) △H2=-56.9kJ/mol查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列说法正确的是( )
| A.第一电离能越小的元素其单质金属活泼性一定越大 |
| B.电负性越小的元素金属性一定越强 |
| C.元素电负性相差小于1.7的元素之间形成的化学键一定为共价键 |
| D.制造光电材料的元素主要从IA族中寻找其主要原因是IA的第一电离能比较低 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
X、Y、Z是原子序数依次递增的短周期元素,3种元素的原子最外层电子数之和与Ca2+的核外电子数相等,Y、Z分别得到一个电子后均形成稀有气体原子的稳定电子层结构。下列说法正确的是
| A.原子半径:Z>Y>X | B.Z与X在同一周期 |
| C.氢化物的稳定性:X>Y | D.XZ4属于共价化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
X、Y、Z、M、W为原子序数依次增大的5种短周期元素。X的质子总数与电子层数相同,Y、Z、M同周期且相邻,W原子核外电子数是M原子最外层电子数的2倍。Z与其同主族的短周期元素可形成常见气体甲。X、Y、Z 3种元素形成化合物乙。下列说法不正确的是
| A.原子半径:W>Y>Z>M>X |
| B.化合物乙中一定只有共价键 |
| C.由W元素形成的单质以及W与Z两元素形成的化合物都是原子晶体 |
| D.X分别与Y、Z、M、W形成的常见化合物中,稳定性最好的是XM,沸点X2Z>XM |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列关于原子结构、元素性质的说法正确的是
| A.原子结构随着元素原子序数的递增而呈周期性变化,这个规律叫元素周期律 |
| B.第三周期元素的简单离子半径随原手序数的递增依次增大 |
| C.第ⅦA族元素的简单阴离子还原性越强,其气态氢化物的稳定性越弱 |
| D.16O2与18O2互为同位素,它们的性质基本相同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com