
| A. | 蜡炬成灰 | B. | 木已成舟 | C. | 铁柱成针 | D. | 滴水成冰 |
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳酸钠固体中含有碳酸氢钠固体,可用灼烧的方法 | |
| B. | 用酚酞溶液可以鉴别饱和食盐水和饱和纯碱溶液 | |
| C. | 25℃,碳酸氢钠在水中的溶解度比碳酸钠的大 | |
| D. | 氢氧化钠与二氧化碳的反应与量有关 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②④ | B. | ①③④ | C. | ②③④ | D. | ①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
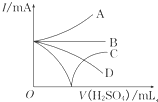 向Ba(OH)2溶液中逐滴加入稀硫酸,请完成下列问题:
向Ba(OH)2溶液中逐滴加入稀硫酸,请完成下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向Al(OH )3胶体中加入酒精溶液能发生聚沉现象 | |
| B. | 豆浆和雾都是胶体 | |
| C. | Fe(OH )3 胶体能透过滤纸 | |
| D. | 向沸水中加入饱和的FeCl3溶液,可制备Fe(OH )3 胶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:钠>硫>氯 | |
| B. | 最高价氧化物对应的水化物的酸性:H3PO4<H2SO4<HClO4 | |
| C. | 最高正化合价:氯>硫>磷 | |
| D. | 热稳定性:碘化氢>溴化氢>氯化氢 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成甲醇:CO(g)+2H2(g)?CH3OH(g).分析该反应并回答下列问题:
甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成甲醇:CO(g)+2H2(g)?CH3OH(g).分析该反应并回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com