
| A£® | ŌČÜŅŗÖŠc£ØFe3+£©=0.2mol•L-1 | |
| B£® | ČÜŅŗÖŠÖĮÉŁÓŠ4ÖÖĄė×Ó“ęŌŚ£¬ĘäÖŠCl”„Ņ»¶Ø“ęŌŚ£¬ĒŅc£ØCl”„£©”Ż0.2mol•L-1 | |
| C£® | SO42”„”¢NH4+”¢Na+Ņ»¶Ø“ęŌŚ£¬CO32”„Ņ»¶Ø²»“ęŌŚ | |
| D£® | ŅŖČ·¶ØŌČÜŅŗÖŠŹĒ·ńŗ¬ÓŠFe2+£¬Ęä²Ł×÷ĪŖ£ŗȔɣĮæŌČÜŅŗÓŚŹŌ¹ÜÖŠ£¬¼ÓČėŹŹĮæĀČĖ®£¬ĪŽĻÖĻó£¬ŌŁ¼ÓKSCNČÜŅŗ£¬ČÜŅŗ³ÉŃŖŗģÉ«£¬Ōņŗ¬ÓŠFe2+ |
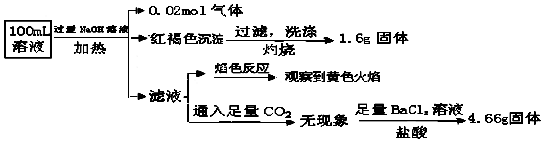
·ÖĪö ¼ÓČė¹żĮæNaOHČÜŅŗ£¬¼ÓČČ£¬µĆµ½0.02molĘųĢ壬øĆĘųĢåĪŖ°±Ęų£¬ŌČÜŅŗÖŠŅ»¶Ø“ęŌŚ0.02molNH4+£»
²śÉśµÄŗģŗÖÉ«³ĮµķĪŖĒāŃõ»ÆĢś£¬1.6g¹ĢĢåĪŖČżŃõ»Æ¶žĢś£¬Ńõ»ÆĢśµÄĪļÖŹµÄĮæĪŖ0.01mol£¬ŌņŌČÜŅŗÖŠŗ¬ÓŠ0.02molĢśŌŖĖŲ£¬æÉÄÜĪŖFe3+”¢Fe2+£¬ŌČÜŅŗÖŠŅ»¶ØƻӊCO32-£»
ĀĖŅŗĶØČė¶žŃõ»ÆĢ¼ĪŽĻÖĻó£¬ŌņŌČÜŅŗÖŠŅ»¶Ø²»“ęŌŚAl3+£»
4.66g²»ČÜÓŚŃĪĖįµÄ¹ĢĢåĪŖĮņĖį±µ£¬ĮņĖį±µµÄĪļÖŹµÄĮæĪŖ0.02mol£¬ŌČÜŅŗÖŠŗ¬ÓŠ0.02molĮņĖįøłĄė×Ó£»
ŃÕÉ«·“Ó¦ĪŖ»ĘÉ«£¬ŌņČÜŅŗÖŠ“ęŌŚÄĘĄė×Ó£¬ÓÉÓŚ¼ÓČėĮĖĒāŃõ»ÆÄĘČÜŅŗ£¬ĪŽ·ØÅŠ¶ĻŌČÜŅŗÖŠŹĒ·ńŗ¬ÓŠÄĘĄė×Ó£»
øł¾ŻČÜŅŗµēÖŠŠŌÅŠ¶ĻŹĒ·ń“ęŌŚĀČĄė×Ó£¬ŅŌ“Ė½ā“šøĆĢā£®
½ā“š ½ā£ŗA£®øł¾ŻŅŌÉĻ·ÖĪöæÉÖŖ£¬ŌČÜŅŗÖŠŗ¬ÓŠ0.02molĢśŌŖĖŲ£¬ĪŽ·ØÅŠ¶Ļ“ęŌŚµÄŹĒĢśĄė×Ó»ņÕßŃĒĢśĄė×Ó£¬¹ŹA“ķĪó£»
B£®øł¾ŻŅŌÉĻ·ÖĪö£¬ŌČÜŅŗÖŠŅ»¶Ø“ęŌŚ0.02molNH4+£¬0.02molSO42-£¬0.02molFe3+”¢Fe2+ÖŠµÄŅ»ÖÖ£¬µ±ĢśŌŖĖŲČ«²æĪŖŃĒĢśĄė×ÓŹ±£¬ŃōĄė×ÓĖł“ųµēŗɵÄĪļÖŹµÄĮæ×īŠ”£¬ĖłŅŌÕżµēŗÉĪļÖŹµÄĮæ×īÉŁĪŖ£ŗ0.02mol”Į2+0.02mol=0.06mol£¬¶ųøŗµēŗɵÄĪļÖŹµÄĮæĪŖ£ŗ0.02mol”Į2=0.04mol£¬øł¾ŻČÜŅŗµēÖŠŠŌæÉÖŖ£¬ŌČÜŅŗÖŠŅ»¶Ø“ęŌŚCl-£¬ĒŅc£ØCl-£©”Ż$\frac{0.06mol-0.04mol}{0.1L}$=0.2 mol•L-1£¬¹ŹBÕżČ·£»
C£®øł¾ŻŅŌÉĻ·ÖĪöæÉÖŖ£¬ŌČÜŅŗÖŠŅ»¶Ø“ęŌŚSO42-”¢NH4+”¢Cl-£¬Ö»ŹĒ“ęŌŚFe3+”¢Fe2+ÖŠµÄŅ»ÖÖ£¬ĘäĄė×ÓµÄĪļÖŹµÄĮæĪŖ0.02mol£¬Ņ»¶Ø²»“ęŌŚCO32-£»ÓÉÓŚµŚŅ»²½ÖŠ¼ÓČėĮĖĒāŃõ»ÆÄĘČÜŅŗ£¬Ņż½ųĮĖÄĘĄė×Ó£¬ĪŽ·ØČ·¶ØŌČÜŅŗÖŠŹĒ·ńŗ¬ÓŠÄĘĄė×Ó£¬¹ŹC“ķĪó£»
D£®¼ģŃéŃĒĢśĄė×ÓŹ±£¬Č”ÉŁĮæŌČÜŅŗÓŚŹŌ¹ÜÖŠ£¬¼ÓKSCNČÜŅŗ£¬“ĖŹ±ČÜŅŗĻÖĻó±ŲŠėŹĒĪŽÉ«£¬Č»ŗóŌŁ¼ÓČėŹŹĮæĀČĖ®£¬ČÜŅŗ³ŹŃŖŗģÉ«£¬Ōņŗ¬ÓŠFe2+£¬·ńŌņČē¹ū¼ÓČėĮņĒč»Æ¼ŲČÜŅŗŗóĻŌŹ¾ŗģÉ«£¬ŌņĪŽ·ØÖ¤Ć÷ŌČÜŅŗÖŠŹĒ·ńŗ¬ÓŠŃĒĢśĄė×Ó£¬¹ŹD“ķĪó£»
¹ŹŃ”£ŗB£®
µćĘĄ ±¾Ģāæ¼²éĪļÖŹ·ÖĄė”¢Ģį“æŹµŃé·½°øµÄÉč¼Ę£¬ĪŖøßĘµæ¼µć£¬°ŃĪÕŹµŃéĮ÷³ĢÖŠµÄŹŌ¼Į”¢·¢ÉśµÄ·“Ó¦¼°·ÖĄė·½·ØĪŖ½ā“šµÄ¹Ų¼ü£¬²ąÖŲ·ÖĪöÄÜĮ¦”¢ŹµŃéÄÜĮ¦µÄ×ŪŗĻ漲飬ĢāÄæÄŃ¶Č²»“ó£¬×¢Ņāøł¾ŻČÜŅŗµēÖŠŠŌÅŠ¶ĻĀČĄė×Ó“ęŌŚµÄ·½·Ø£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
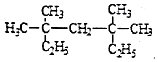 ĻµĶ³ĆüĆū·ØĪŖ3£¬3£¬5£¬5-Ėļ׻łøżĶ飻
ĻµĶ³ĆüĆū·ØĪŖ3£¬3£¬5£¬5-Ėļ׻łøżĶ飻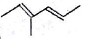 ±ķŹ¾µÄÓŠ»śĪļµÄ½į¹¹¼ņŹ½ŹĒCH3CH=C£ØCH3£©CH=CHCH3£»
±ķŹ¾µÄÓŠ»śĪļµÄ½į¹¹¼ņŹ½ŹĒCH3CH=C£ØCH3£©CH=CHCH3£»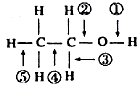
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
 ČēĶ¼ŹĒÄ³Ń§Š£ŹµŃéŹŅ“Ó»ÆѧŹŌ¼ĮÉĢµźĀņ»ŲµÄĮņĖįŹŌ¼Į±źĒ©ÉĻµÄ²æ·ÖÄŚČŻ£®
ČēĶ¼ŹĒÄ³Ń§Š£ŹµŃéŹŅ“Ó»ÆѧŹŌ¼ĮÉĢµźĀņ»ŲµÄĮņĖįŹŌ¼Į±źĒ©ÉĻµÄ²æ·ÖÄŚČŻ£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 £¬·“Ó¦ĄąŠĶĪŖõ„»Æ·“Ó¦£®
£¬·“Ó¦ĄąŠĶĪŖõ„»Æ·“Ó¦£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĶʶĻĢā
| A | C | |
| B |
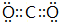 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĮņĒčĖį¼ŲČÜŅŗ | B£® | ĻõĖį | ||
| C£® | ĖįŠŌøßĆĢĖį¼ŲČÜŅŗ | D£® | ĀČĖ® |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
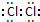 £»
£»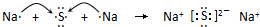 £®
£®²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com