
【题目】工业上通常以2异丙基苯酚(A)为原料,生产一种常用的农药——扑灭威(B),过程如下:
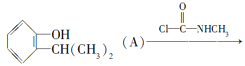
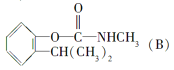
下列有关说法错误的是( )
A.上述反应属于取代反应
B.B在强酸、强碱性环境中都不能稳定存在
C.A与B可用FeCl3溶液进行鉴别
D.1molB在NaOH溶液中水解,最多消耗2molNaOH
【答案】D
【解析】
A. 根据A与B两种物质结构的差异分析;
B. B物质中存在酯基和肽键,在酸性或碱性条件下均可发生水解反应;
C. 酚类物质遇到FeCl3溶液显紫色;
D. -COO-、-CONH-以及水解生成的酚羟基均可与碱发生反应。
A. A中酚羟基变为了B中的![]() ,即-OH中的氢原子被
,即-OH中的氢原子被![]() 替代,因此发生了取代反应,A项正确,不符合题意;
替代,因此发生了取代反应,A项正确,不符合题意;
B. B物质中存在酯基和肽键,在酸性或碱性条件下均可发生水解反应,因此B在强酸、强碱性环境中都不能稳定存在,B项正确,不符合题意;
C. 酚类物质遇到FeCl3溶液显紫色,A中含有酚羟基,B中不含酚羟基,因此可以用FeCl3溶液进行鉴别,C项正确,不符合题意;
D. -COO-、-CONH-以及水解生成的酚羟基均可与碱发生反应,因此1molB在NaOH溶液中水解,可以消耗3molNaOH,D项错误,符合题意;
答案选D。


 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案 新思维寒假作业系列答案
新思维寒假作业系列答案科目:高中化学 来源: 题型:
【题目】在容积不变的密闭容器中,一定条件下发生反应:2A(?) ![]() B(g)+2C(g),且达到平衡。当升高温度时气体的密度增大,则下列叙述中正确的是 ( )
B(g)+2C(g),且达到平衡。当升高温度时气体的密度增大,则下列叙述中正确的是 ( )
A.升高温度,正反应速率增大,逆反应速率减小B.若正反应是放热反应,则A为气态
C.物质A一定为非气态,且正反应是吸热反应D.若向容器中充入惰性气体,则平衡向左移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中进行如下反应 X2(g)+Y2(g) ![]() 2Z(g),已知X2、Y2、Z的起始浓度分别为0.1mol/L、0.3mol/L、0.2mol/L,在一定条件下,当反应达到平衡时,各物质的浓度可能为
2Z(g),已知X2、Y2、Z的起始浓度分别为0.1mol/L、0.3mol/L、0.2mol/L,在一定条件下,当反应达到平衡时,各物质的浓度可能为
A. Y2为0.4mol/LB. Z为0.3mol/L
C. X2为0.2mol/LD. Z为0.4mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 a、b、c、d是四种短周期元素。a、b、d同周期,c、d同主族。a的原子结构示意图为
 , b与c形成化合物的电子式为
, b与c形成化合物的电子式为![]() 。下列比较中正确的是( )
。下列比较中正确的是( )
A. 原子半径:a>c>d>b B. 电负性a>b>d>c
C. 原子序数:d>a>c>b D. 最高价含氧酸的酸性c>d>a
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组用图示装置制备高铁酸钾(K2FeO4)并探究其性质。已知:K2FeO4为紫色固体,微溶于KOH溶液;具有强氧化性,在酸性或中性溶液中快速产生O2,在碱性溶液中较稳定。制取实验完成后,取C中紫色溶液,加入稀盐酸,产生气体。下列说法不正确的是

A.B瓶应盛放饱和食盐水除去混有的HCl
B.C瓶中KOH过量更有利于高铁酸钾的生成
C.加盐酸产生气体可说明氧化性:K2FeO4>Cl2
D.高铁酸钾是集氧化、吸附、絮凝、沉淀、灭菌、消毒、脱色、除臭等八大特点为一体的优良的水处理剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇可作为燃料电池的原料。CO2和CO可作为工业合成甲醇(CH3OH)的直接碳源,
(1)已知在常温常压下:
①CH3OH(l)+ O2(g)=CO(g) + 2H2O(g); ΔH=﹣355.0 kJ∕mol
②2CO(g)+ O2(g)= 2CO2(g) ΔH=-566.0 kJ/mol
③H2O(l)=H2O(g) ΔH=+44.0 kJ/mol
写出表示甲醇燃烧热的热化学方程式:___________________________
(2)利用CO和H2在一定条件下可合成甲醇,发生如下反应:CO(g)+2H2(g)=CH3OH(g),其两种反应过程中能量的变化曲线如下图a、b所示,下列说法正确的是__________
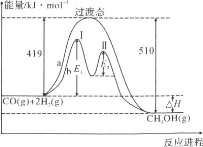
A.上述反应的ΔH=-91kJ·mol-1
B.a反应正反应的活化能为510kJ·mol-1
C.b过程中第Ⅰ阶段为吸热反应,第Ⅱ阶段为放热反应
D.b过程使用催化剂后降低了反应的活化能和ΔH
E.b过程的反应速率:第Ⅱ阶段>第Ⅰ阶段
(3)下列是科研小组设计的一个甲醇燃料电池,两边的阴影部分为a,b惰性电极,分别用导线与烧杯的m,n相连接,工作原理示意图如图:
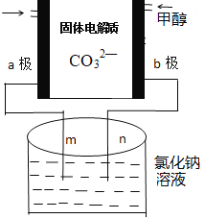
①b极电极反应式为____________。
②在标准状况下,若通入112mL的O2,(假设烧杯中的溶液的体积为200mL,体积不变)最后反应终止时烧杯中溶液的pH为______。
(4)可利用CO2根据电化学原理制备塑料,既减少工业生产对乙烯的依赖,又达到减少CO2排放的目的。以纳米二氧化钛膜为工作电极,稀硫酸为电解质溶液,在一定条件下通入CO2进行电解,在阴极可制得低密度聚乙烯![]() (简称LDPE)。
(简称LDPE)。
①电解时,阴极的电极反应式是________。
②工业上生产1.4×102kg的LDPE,理论上需要标准状况下________L的CO2。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】尿黑酸是由酪氨酸在人体内非正常代谢而产生的一种物质。其转化过程如下:

下列说法错误的是( )
A.对羟基苯丙酮酸分子中在同一平面上的碳原子至少有7个
B.1mol尿黑酸与足量NaHCO3反应,最多消耗3molNaHCO3
C.酪氨酸既能与盐酸反应,又能与氢氧化钠反应
D.1mol尿黑酸与足量浓溴水反应,最多消耗3mol Br2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组在实验室探究过渡金属元素化合物的性质
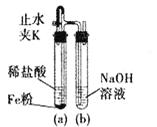
(1)向![]() 溶液中滴加NaOH溶液,产生白色沉淀,但迅速变为灰绿色,最终变为红褐色,为顺利看到较长时间的白色沉淀,设计了如图装置:①检查装置气密性,装入药品;②打开止水夹K;③在试管b出口收集气体并验纯;④关闭止水夹K。以上操作正确的顺序是:________。
溶液中滴加NaOH溶液,产生白色沉淀,但迅速变为灰绿色,最终变为红褐色,为顺利看到较长时间的白色沉淀,设计了如图装置:①检查装置气密性,装入药品;②打开止水夹K;③在试管b出口收集气体并验纯;④关闭止水夹K。以上操作正确的顺序是:________。
(2)某实验小组称量![]() 草酸亚铁晶体
草酸亚铁晶体![]() 加热过程中,固体质量变化如图所示:
加热过程中,固体质量变化如图所示:
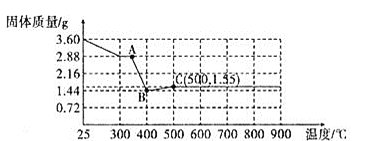
①请写出AB段发生反应的化学方程式:________________。
②![]() 点成分为:________。
点成分为:________。
(3)向![]() 溶液中加入过量
溶液中加入过量![]() 溶液,设计实验证明两者发生了氧化还原反应并且为可逆反应。
溶液,设计实验证明两者发生了氧化还原反应并且为可逆反应。![]() 简要说明实验步骤、现象和结论,仪器和药品自选
简要说明实验步骤、现象和结论,仪器和药品自选![]() ________________。
________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某恒容密闭容器中充入一定量SO2和O2进行反应: 2SO2(g)+O2(g)![]() 2SO3(g) ΔH<0,图甲表示反应速率(v)与温度(T) 的关系、图乙表示 T1 时,平衡体系中SO2的体积分数与压强(p)的关系。下列说法正确的是( )
2SO3(g) ΔH<0,图甲表示反应速率(v)与温度(T) 的关系、图乙表示 T1 时,平衡体系中SO2的体积分数与压强(p)的关系。下列说法正确的是( )
图甲 ,图乙
,图乙
A.图甲中,曲线1表示正反应速率与温度的关系
B.图乙中,a、b两点的反应速率:v(a)>v(b)
C.图甲中,d点时,混合气体的平均摩尔质量不再改变
D.图乙中,c点的正、逆反应速率:v(逆) < v(正)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com