
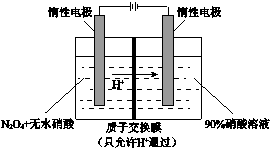
| A. | 阳极电解液中的N2O4可由NO2降温转化制得 | |
| B. | 阳极的电极反应为:N2O4-2e-+2HNO3=2N2O5+2H+ | |
| C. | 阴极的电极反应为:2H++2e-=H2↑ | |
| D. | 每制备1molN2O5,有1molH+通过质子交换膜 |
分析 A.NO2(g)?N2O4(g)△H<0;
B.阳极上N2O4失电子生成N2O5;
C.阴极上氢离子得电子生成氢气;
D.根据电极方程式结合电荷守恒分析.
解答 解:A.NO2(g)?N2O4(g)△H<0,降低温度向吸热方向移动,即降低温度向生成N2O4的方向移动,故A正确;
B.阳极上N2O4失电子生成N2O5,则阳极电极方程式为:N2O4-2e-+2HNO3=2N2O5+2H+,故B正确;
C.阴极上氢离子得电子生成氢气,则阴极上电极方程式为:2H++2e-=H2↑;
D.已知阳极电极方程式为:N2O4-2e-+2HNO3=2N2O5+2H+,阴极上电极方程式为:2H++2e-=H2↑,则每制备1molN2O5,转移2mol电子,所以溶液中有2molH+通过质子交换膜,故D错误.
故选D.
点评 本题主要考查电解池的工作原理,注意阳极发生氧化反应,阴极发生还原反应,题目难度中等,明确电解池中电极的判断以及电极方程式的书写是解题的关键,侧重于考查学生的分析能力和计算能力.


科目:高中化学 来源: 题型:选择题
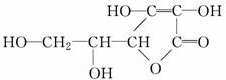
| A. | 易起氧化及加成反应 | B. | 在碱性溶液中不能稳定地存在 | ||
| C. | 难溶解于水 | D. | 是一个环状的酯类化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯的结构简式:CH2=CH2 | B. | 醋酸的分子式:CH3COOH | ||
| C. | 丙烷的比例模型: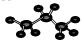 | D. | 乙酸甲酯的结构式:CH3COOCH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该溶液中Na+、K+、NO${\;}_{3}^{-}$、Cl-可大量共存 | |
| B. | 向溶液中通入CO2气体可以增强溶液漂白性 | |
| C. | 和浓盐酸反应的离子方程式:Cl-+ClO-+2H+=Cl2↑+H2O | |
| D. | 通入过量SO2气体反应的离子方程式:SO2+ClO-+Ca2++H2O=CaSO4↓+Cl-+2H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蔗糖、淀粉、油脂及其水解产物均为非电解质 | |
| B. | 沼气的利用,玉米制乙醇都涉及生物质能的利用 | |
| C. | 氨氮废水(含NH4+及NH3)可用化学氧化法或电化学氧化法处理 | |
| D. | pH计可用于酸碱中和滴定终点和乙酸乙酯的水解程度的判断 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
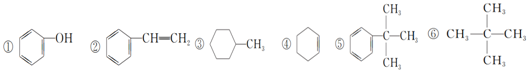
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 锥形瓶在装待测液前要用待测液润洗2~3次 | |
| B. | 用25mL酸式滴定管量取20.00mLKMnO4溶液 | |
| C. | 测某溶液pH:用蒸馏水润湿pH试纸,然后用洁净干燥的玻璃棒蘸取试样进行检测 | |
| D. | 加热蒸发NaHCO3溶液得纯净的NaHCO3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com