
| A. | 冬天,5%H2O2溶液分解 | B. | 冬天,MnO2与5%H2O2溶液混合 | ||
| C. | 夏天,5%H2O2溶液分解 | D. | 夏天,MnO2与5%H2O2溶液混合 |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe3O4溶于足量稀HNO3:Fe3O4+8H+═Fe2++2Fe3++4H2O | |
| B. | 将过量的SO2通入Ca(ClO)2溶液中:SO2+ClO-+H2O═HClO+HSO3- | |
| C. | 向MgSO4溶液中滴加Ba(OH)2溶液:Ba2++SO42-═BaSO4↓ | |
| D. | 向NH4HSO4稀溶液中逐滴加入Ba(OH)2稀溶液至SO42-刚好沉淀完全:Ba2++2OH-+NH4++H++SO42-═BaSO4↓+NH3•H2O+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯不能使KMnO4溶液褪色,因此苯不能发生氧化反应 | |
| B. | 丙烯分子中最多有6个原子共平面 | |
| C. | 甲苯硝化制对硝基甲苯与苯甲酸和乙醇反应制苯甲酸乙酯的反应类型不同 | |
| D. | 乙醇、乙酸、乙酸乙酯都能发生取代反应,除去乙酸乙酯中乙酸可用饱和碳酸钠溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ②③④ | C. | ①③⑥ | D. | ③⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
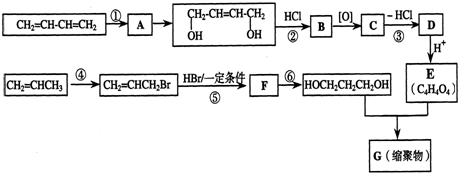
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 根据同周期元素的第一电离能变化趋势,推出Al的第一电离能比Mg大 | |
| B. | 根据较强酸可以制取较弱酸的规律,推出CO2通入NaClO溶液中能生成HClO | |
| C. | 根据溶液的pH与溶液酸碱性的关系,推出pH=6.8的溶液一定显酸性 | |
| D. | 根据主族元素最高正化合价与族序数的关系,推出卤族元素最高正价都是+7 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com