
【题目】设NA为阿伏加德罗常数的值,下列有关说法正确的是
A.46g N2O4气体中含有的原子数为3NA
B.标准状况下,22.4L SO3中含有SO3分子数为NA
C.50mL 12mol·L-1盐酸与足量MnO2共热,转移的电子数为0.3NA
D.用电解法精炼铜的反应中转移0.2NA个电子时,阳极溶解6.4g铜
 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案科目:高中化学 来源: 题型:
【题目】汽车尾气里含有NO气体是由于内燃机燃烧的高温引起氮气和氧气反应所致:N2(g) + O2(g) ![]() 2NO(g) △H>0,已知该反应在某温度时,平衡常数K = 6.4×10-3。回答:
2NO(g) △H>0,已知该反应在某温度时,平衡常数K = 6.4×10-3。回答:
(1)某温度下,向2 L的密闭容器中充入N2和O2各1 mol,5分钟后O2的物质的量为0.6 mol,则N2的反应速率为_______________。
(2)假定该反应是在恒温、恒压条件下进行,判断该反应达到平衡的标志_______(填字母序号)。
A、混合气体密度不变
B、消耗1 mol N2同时消耗2 mol NO
C、混合气体平均相对分子质量不变
D、2υ正(N2) = υ逆(NO)
(3)将N2、O2的混合气体充入恒温恒容密闭容器中,下列变化趋势不正确的是_______(填字母序号)。

(4)向恒温恒容的密闭容器中充入等物质的量的N2和O2,达到平衡状态后再向其中充入一定量NO,重新达到化学平衡状态。与原平衡状态相比,此时平衡混合气体中NO的体积分数______(填“变大”、“变小”或“不变”)。
(5)该温度下,某时刻测得容器内N2、O2、NO的浓度分别为2.5×10-1 mo1/L、4.0×10-2 mo1/L和8.0×10-2 mo1/L,此时反应_____________(填“处于化学平衡状态”、“向正反应方向进行”或“向逆反应方向进行”),理由是____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】上海某一超市销售的某种食用精制盐包装袋上有如下说明:

(1)碘酸钾与碘化钾在酸性条件下发生如下反应,配平化学方程式并画出电子转移的方向与数目:_____KIO3+_____KI+_____H2SO4=_____K2SO4+_____I2+_____H2O;电子转移情况如下(双线桥表示)__________________________________;
(2)上述反应生成的I2可用叫氯化碳萃取,并用分液漏斗分离出两种溶液。其实验操作可分解为如下几步:
A.把盛有溶液的分液漏斗放在铁架台的铁圈中;
B.把50mL碘水和15mL CCL4加入分液漏斗中,并盖好玻璃塞;
C.检验分液漏斗活塞上的玻璃塞是否漏液;
D.倒转漏斗用力振荡,并不时旋开活塞放气,最后关闭活塞,把分液漏斗方正;
E.旋开活塞,用烧杯接收溶液;
F.从分液漏斗的上口倒出上层水溶液;
G.静置,分层。
a、正确的操作顺序是(用编号字母填写)_____→_____→_____→A→_____→_____E→F。
b、下列物质。还能用作从溶液中萃取碘的溶剂是_____。
A.苯 B.碘化钾 C.酒精
(3)若向碘的四氯化碳溶液中加入Na2SO3稀溶液,将I2还原,以回收四氯化碳。Na2SO3稀溶液与I2反应的主要产物(化学式)是_____。
(4)已知:I2+2Na2S2O3=2NaI+Na2S4O6.某学生测定食用精制盐的碘含量,其步骤为:
a.准确称取wg食盐,加适量蒸馏水使其完全溶解;
b.用稀硫酸酸化所得溶液,加入过量KI溶液,使KIO3与KI反应完全;
c.以淀粉溶液为指示剂,逐滴加入物质的量浓度为2.0×10-3mol/L的Na2S2O3溶液15.00mL,恰好反应完全。
①判断c中反应恰好完全依据的现象是_____。
②根据以上实验和包装袋说明,所测精制盐的碘含量是(以含w的代数式表示)_____mg/kg。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)3.01×1023个氯气分子的物质的量是________,氯原子的物质的量是________。
(2)1.5mol Na2SO4·10H2O中所含的Na+的物质的量是________,所含的SO42-的物质的量是________,所含H2O的数目是______。
(3)一定量的Na2CO3中,碳原子和氧原子的物质的量之比为______。
(4)0.5mol NaOH中含有电子的物质的量是__________,在________mol Na2CO3中所含Na+数目与上述0.5mol NaOH所含Na+数目相等。
(5)12.4g Na2R含0.4mol Na+,则Na2R的摩尔质量为_______,R的相对原子质量为________。含R的质量为1.6g的Na2R,其物质的量为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种新型钠硫电池结构示意图如图,下列有关该电池的说法正确的是

A.电池放电时,Na+向电极A极移动
B.电池放电时,A极电极反应为2Na++xS+2e-= Na2Sx
C.电池充电时,B接负极
D.电池充电时,每转移1mol电子将有1mol Na+被还原
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮(N)、磷(P)、砷(As)等都是VA族的元素,该族元素的化合物在研究和生产中有许多重要用途。回答下列问题:
(1)NH3的沸点比PH3高,原因是________________________________________________。
(2)Na3AsO4 中含有的化学键类型包括________________________;AsO43-的空间构型为____________(用文字描述)。
(3)NH3和F2在Cu催化下可发生反应4NH3+3F2=NF3+3NH4F,化学方程式中的5种物质所属的晶体类型有_____________________(填序号)。写出基态铜原子的价电子排布式_______________。
a.离子晶体 b.分子晶体 c.原子晶体 d.金属晶体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个不导热的恒容密闭容器中通入CO(g)和H2O(g),一定条件下使反应CO(g)+H2O(g)![]() CO2(g)+H2(g)达到平衡状态,正反应速率随时间变化的示意图如图所示。由图可得出的正确结论是
CO2(g)+H2(g)达到平衡状态,正反应速率随时间变化的示意图如图所示。由图可得出的正确结论是
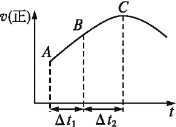
A.反应物浓度:A点小于C点
B.该反应的正反应为吸热反应
C.C点时反应进行的程度最大
D.Δt1=Δt2时,生成H2的物质的量:AB段小于BC段
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮的化合物在化肥、医药、炸药、材料等领域中有着极其重要用途。
(1)羟氨能与溴化银悬浊液反应:2NH2OH+2AgBr=N2↑+2Ag+2HBr+2H2O,羟氨的电子式为________;反应中烃氨表现________性.
(2)已知:a.N2(g)+3H2(g)=2NH3(g) △H=-92.2kJ/mol
b.H2(g)+Cl2(g)=2HCl(g) △H=-184.6kJ/mol
c.2NH3(g)+3Cl2(g)=N2(g)+6HCl(g) △H3
①△H3________.
②反应c在常温下能快速进行的原因为________.
(3)容积均为1L的甲、乙两个容器,其中甲为绝热容器,乙为恒温容器.相同温度下,分别充入0.2mol的NO2,发生反应:2NO2(g)≒N2O4(g) △H<0,甲中NO2的相关量随时间变化如下图所示。
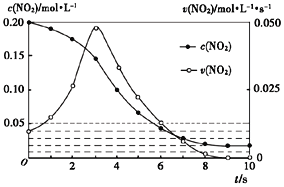
①0~3S内,甲容器中NO2的反应速率增大的原因是________.
②甲达平衡时,温度若为T℃,此温度下的平衡常数Kc=________.
③平衡时,K甲________K乙(填“>”、“<”或“=”,下同),P甲________P乙
(4)化学工作者对NO与H2的反应进行研究,提出下列3步机理:(k为速率常数)
第一步2NO=N2O2 快反应,平衡时:V正=K正·c2(NO)=V逆=K逆·c(N2O2)
第二步N2O2+H2==N2O+H2O 慢反应 第三步N2O+H2=N2+H2O 快反应
其中可近似认为第二步反应不影响第一步平衡,下列说法正确的是________.(填字母标号)
A.V(第一步逆反应)<V(第二步反应) B.总反应快慢主要由第二步反应决定
C.达平衡时,2c(NO)=c(N2O2) D.第一步反应的平衡常数K= K正/ K逆
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com