
求算下列常温下溶液中由H2O电离的c(H+)和c(OH-)。
(1)pH=2的H2SO4溶液
c(H+)=__________,c(OH-)=__________。
(2)pH=10的NaOH溶液
c(H+)=__________,c(OH-)=__________。
(3)pH=2的NH4Cl溶液
c(H+)=__________。
(4)pH=10的Na2CO3溶液
c(OH-)=__________。
答案 (1)10-12 mol·L-1 10-12 mol·L-1
(2)10-10 mol·L-1 10-10 mol·L-1 (3)10-2 mol·L-1
(4)10-4 mol·L-1
解析 (1)pH=2的H2SO4溶液中,H+来源有两个:H2SO4的电离和H2O的电离,而OH-只来源于水。应先求算c(OH-),即为水电离的c(H+)或c(OH-)。
(2)pH=10的NaOH溶液中,OH-有两个来源:H2O的电离和NaOH的电离,H+只来源于水。应先求出c(H+),即为水电离的c(OH-)或c(H+),c(OH-)=10-4 mol·L-1,c(H+)=10-10 mol·L-1,则水电离的c(H+)=c(OH-)=10-10 mol·L-1。
(3)(4)水解的盐溶液中的H+或OH-均由水电离产生,水解显酸性的盐应计算其c(H+),水解显碱性的盐应计算其c(OH-)。pH=2的NH4Cl中由水电离产生的c(H+)=10-2 mol·L-1;pH=10的Na2CO3溶液中由水电离产生的c(OH-)=10-4 mol·L-1。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
下列叙述正确的是( )
A.铝制容器可盛装热的浓硫酸
B.镁的金属性比铝的金属性强
C.氢氧化铝能溶于过量氨水
D.镁在空气中燃烧生成的固体只有MgO
查看答案和解析>>
科目:高中化学 来源: 题型:
使用微波炉加热,具有使受热物质均匀、表里一致、速度快、热效率高等优点。其工作原理是通电炉内的微波场以几亿的高频改变电场的方向,水分子因而能迅速摆动,产生热效应,这是因为( )
A.水分子具有极性共价键
B.水分子中有共用电子对
C.水由氢、氧两元素组成
D.水分子是极性分子
查看答案和解析>>
科目:高中化学 来源: 题型:
以下说法正确的是( )
①若把H2S分子写成H3S分子,违背了共价键的饱和性 ②H3O+离子的存在,说明共价键不应有饱和性 ③所有的共价键都有方向性 ④只有化合物中才存在离子键和极性共价键
A.①② B.②④
C.①③ D.①④
查看答案和解析>>
科目:高中化学 来源: 题型:
处于前三周期的主族元素A、B、C、D,其离子半径逐渐增大,它们的原子中核外都有一个未成对电子。已知A和D处于同一周期,0.2 mol A单质可以从D的氢化物的水溶液中置换出6.72 L H2(标准状况),试回答:
(1)写出元素符号:
A.________,B.________,C.________,D.________;
(2)若C有气态氢化物存在,比较C和D的氢化物:
沸点__________,稳定性__________,水溶液的酸性____________;
(3)四种元素的第一电离能由大到小的排列顺序是________________________;
(4)四种元素的电负性由小到大的顺序是______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某小组以CoCl2·6H2O、NH4Cl、H2O2、浓氨水为原料,在活性炭催化下,合成了橙黄色晶体X,为确定其组成,进行如下实验。
①氨的测定:精确称取w g X,加适量水溶解,注入如图所示的三颈瓶中,然后逐滴加入足量10% NaOH溶液,通入水蒸气,将样品液中的氨全部蒸出,用V1 mL c1 mol·L-1的盐酸标准溶液吸收。蒸氨结束后取下接收瓶,用c2 mol·L-1 NaOH标准溶液滴定过剩的HCl,到终点时消耗V2 mL NaOH溶液。
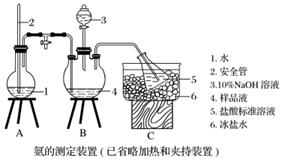
②氯的测定:准确称取样品X,配成溶液后用AgNO3标准溶液滴定,K2CrO4溶液为指示剂,至出现淡红色沉淀不再消失为终点(Ag2CrO4为砖红色)。
回答下列问题:
(1)装置中安全管的作用原理是_____________________________________________
________________________________________________________________________。
(2)用NaOH标准溶液滴定过剩的HCl时,应使用______式滴定管,可使用的指示剂为________。
(3)样品中氨的质量分数表达式为________________。
(4)测定氨前应该对装置进行气密性检验,若气密性不好测定结果将________(填“偏高”或“偏低”)。
(5)测定氯的过程中,使用棕色滴定管的原因是_____________________________________;滴定终点时,若溶液中c(Ag+)=2.0×10-5 mol·L-1,c(CrO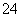 )为________ mol·L-1。[已知:Ksp(Ag2CrO4)=1.12×10-12]
)为________ mol·L-1。[已知:Ksp(Ag2CrO4)=1.12×10-12]
(6)经测定,样品X中钴、氨和氯的物质的量之比为1∶6∶3,钴的化合价为________。制备X的化学方程式为______________________________________________________
________________________________________________________________________;
X的制备过程中温度不能过高的原因是____________________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
有机物G是一种食品香料,其香气强度为普通香料的3~4倍,有机物G的合成路线如下: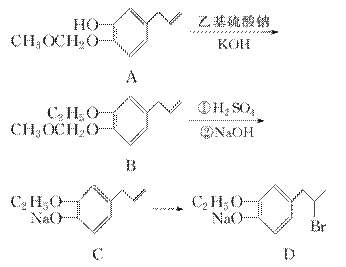
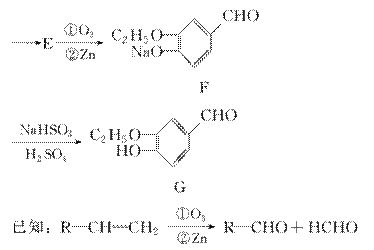
(1)该香料长期暴露于空气中易变质,其原因是__________________________________________________________________________________________________________________________________________。
(2)写出A中含氧官能团的名称:________,由C到 D的反应类型为________。
(3)有机物E的结构简式为________________________________________________________________________。
(4)有机物G同时满足下列条件的同分异构体有____________种。
①与FeCl3溶液反应显紫色;
②可发生水解反应,其中一种水解产物能发生银镜反应;
③分子中有4种不同化学环境的氢。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com