
| A. | Ca(HCO3)2溶液与足量盐酸混合:Ca(HCO3)2+2H+═Ca2++2CO2↑+2H2O | |
| B. | Na2CO3溶液中通入CO2气体:CO${\;}_{3}^{2-}$+CO2+H2O═2HCO${\;}_{3}^{-}$ | |
| C. | 实验室用NH4Cl固体与Ca(OH)2固体混合制NH3:NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O | |
| D. | 将SO2气体通入NaClO溶液中:SO2+2ClO-+H2O=SO${\;}_{3}^{2-}$+2HClO |
分析 A.碳酸氢钙为可溶性盐,拆成离子形式;
B.反应生成碳酸氢钠;
C.氯化铵固体、氢氧化钙固体书写离子方程式应保留化学式;
D.二氧化硫能够被次氯酸根离子氧化生成硫酸根离子.
解答 解:A.Ca(HCO3)2溶液与足量盐酸混合,离子方程式:HCO3-+H+═+CO2↑+H2O,故A错误;
B.Na2CO3溶液中通入CO2气体,离子方程式:CO${\;}_{3}^{2-}$+CO2+H2O═2HCO${\;}_{3}^{-}$,故B正确;
C.实验室用NH4Cl固体与Ca(OH)2固体混合制NH3,离子方程式:2NH4Cl(固)+Ca(OH)2(固) $\frac{\underline{\;\;△\;\;}}{\;}$ CaCl2+2NH3↑+2H2O,故C错误;
D.NaClO溶液中通入过量SO2气体的离子反应为ClO-+H2O+SO2═2H++Cl-+SO42-,故D错误;
故选:B.
点评 本题考查了离子方程式书写,明确离子方程式书写方法及发生反应的实质是解题关键,注意物质化学式的拆分,题目难度不大.


科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
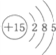 ,下列说法正确的是( )
,下列说法正确的是( )| A. | 该原子位于第三周期,ⅤA族 | B. | 该原子位于第五周期,ⅢB族 | ||
| C. | 该原子位于第三周期,ⅤB族 | D. | 该原子位于第五周期,ⅢA族 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 已知A、B、C、D、E五种元素均位于周期表的前四周期,且原子序数依次增大.元素A是周期表中原子半径最小的元素;B的基态原子中电子占据了三种能量不同的原子轨道,且这三种轨道中的电子数相同;D位于第2周期,其原子核外成对电子数是未成对电子数的3倍;E位于ds区,且原子的最外层电子数与A的相同.
已知A、B、C、D、E五种元素均位于周期表的前四周期,且原子序数依次增大.元素A是周期表中原子半径最小的元素;B的基态原子中电子占据了三种能量不同的原子轨道,且这三种轨道中的电子数相同;D位于第2周期,其原子核外成对电子数是未成对电子数的3倍;E位于ds区,且原子的最外层电子数与A的相同.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④ | B. | 只有②③④ | C. | 只有①③④ | D. | 只有②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 生成氢气的速率从快到慢为④③②① | |
| B. | 四组实验反应完全后生成氢气的总量相等 | |
| C. | 四组实验反应完全后锌均无剩余 | |
| D. | 四组实验反应完全后所得的硫酸锌的物质的量相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
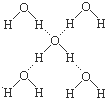 下列有关冰的说法中,正确的组合是( )
下列有关冰的说法中,正确的组合是( )| A. | 除⑥外 | B. | 除④外 | C. | 除④⑤⑥外 | D. | 全对 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2.5 mol | B. | 2 mol | C. | 1.25 mol | D. | 0.5 mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com