
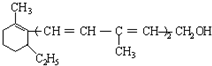
| A. | 维生素A是一种烯烃 | |
| B. | 维生素A的一个分子中有30个氢原子 | |
| C. | 维生素A的一个分子中有五个双键 | |
| D. | 维生素A能使溴水褪色,能被酸性KMnO4氧化 |
分析 由结构可知,分子中含C、H、O三种元素,含碳碳双键、-OH,结合烯烃及醇的性质来解答;分析维生素A的结构简式可知,分子中不含苯环,含有5个C=C键和1个-OH,结合有机物的结构解答该题.
解答 解:A.只有碳氢两种元素组成的化合物是烃,维生素A中含有氧元素,不是烃,故A错误;
B.由结构简式可知维生素A的一个分子中含有30个H原子,故B正确;
C.由结构简式可知维生素A的一个分子中有5个C=C键双键,故C正确;
D.维生素A中含有碳碳双键,能与溴水发生加成褪色,也能被酸性KMnO4溶液氧化,故D正确,
故选A.
点评 本题考查有机物的结构和性质,为高频考点,难度不大.把握官能团与性质的关系为解答的关键,


科目:高中化学 来源: 题型:选择题
| A. | 硫的原子结构示意图: | |
| B. | Be2+离子中的质子数和电子数之比为2:1 | |
| C. | 原子核内有8个中子的碳原子:${\;}_{8}^{14}$C | |
| D. | 同一元素的各种同位素的物理性质、化学性质均相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
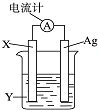 依据氧化还原反应:2Ag++Cu═Cu2++2Ag设计的原电池如图所示.请回答下列问题:
依据氧化还原反应:2Ag++Cu═Cu2++2Ag设计的原电池如图所示.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 能源是现代社会发展的支柱之一,化学能是重要的能源.
能源是现代社会发展的支柱之一,化学能是重要的能源.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用福尔马林保存生物标本 | |
| B. | 试管上沾有苯酚时,用水洗 | |
| C. | 实验室不慎将Hg洒在地上时,立即用硫粉覆盖 | |
| D. | 皮肤上沾有苯酚时,立即用酒精擦洗 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径 Z>Y>X | |
| B. | Z的非金属性最强 | |
| C. | 氢化物还原性XH3>H2Y>HZ,稳定性XH3>H2Y>HZ | |
| D. | 最高氧化物对应水化物H3XO4酸性最强 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com