
����Ŀ����֪�л���A��һ����Ҫ�Ļ���ԭ�ϣ�ת����ϵ����ͼ:
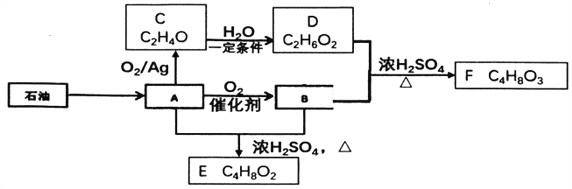
��֪:ͬһ̼ԭ��������2����2������-OH�Dz��ȶ��ṹ��E�ܷ���ˮ�ⷴӦ
��ش�:
��1��A���������________��
��2���л���C�Ľṹ��ʽ________��
��3��B+D-F�Ļ�ѧ����ʽ��________��
��4����֪![]() �ܰ���ͼ��ʽ�����ѽ�:
�ܰ���ͼ��ʽ�����ѽ�:
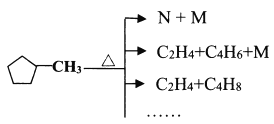
����˵������ȷ����________��
A.������ˮ����![]() ��N
��N
B.E��![]() ������ʹ����KMnO4��ɫ
������ʹ����KMnO4��ɫ
C.��������A��![]() ��ȫȼ��ʱ�ĺ�������ͬ
��ȫȼ��ʱ�ĺ�������ͬ
D.N(��Ԫ��)���ܵĽṹ��3��
���𰸡� ̼̼˫�� ![]() HOCH2��CH2OH+CH3COOH
HOCH2��CH2OH+CH3COOH![]() CH3COOCH2CH2OH+H2O BD
CH3COOCH2CH2OH+H2O BD
�����������⿼���л�����ƶϣ�A��һ����Ҫ�Ļ���ԭ�ϣ���A����ʯ�͵õ�����A������C�����AΪ��ϩ�����ṹ��ʽΪCH2=CH2��E����ʽΪC4H8O2����E����A��B��Ũ����������£����ɣ���EΪ�����ṹ��ʽΪCH3COOCH2CH3��BΪCH3COOH��D��E��Ũ���������·�Ӧ����F���Լ�F�Ľṹ��ʽ���Ƴ�FΪ������DΪCH3CH2OH����C�Ľṹ��ʽΪ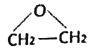 ����1��A�к��еĹ�������̼̼˫������2����������������C�Ľṹ��ʽΪ
����1��A�к��еĹ�������̼̼˫������2����������������C�Ľṹ��ʽΪ ����3������F�ķ���ʽ��B��D��Ӧ�ķ���ʽΪ HOCH2��CH2OH+CH3COOH
����3������F�ķ���ʽ��B��D��Ӧ�ķ���ʽΪ HOCH2��CH2OH+CH3COOH![]() CH3COOCH2CH2OH+H2O����4��
CH3COOCH2CH2OH+H2O����4��![]() ����C2H4��C4H6��M������Ԫ���غ��ԭ���غ㣬�Ƴ�MΪH2��
����C2H4��C4H6��M������Ԫ���غ��ԭ���غ㣬�Ƴ�MΪH2��![]() ����N��M���Ƴ�N�ķ���ʽΪC6H10����N�к���̼̼˫����A��
����N��M���Ƴ�N�ķ���ʽΪC6H10����N�к���̼̼˫����A��![]() ����̼̼˫��������ʹ��ˮ��ɫ��N�к���̼̼˫������ʹ��ˮ��ɫ����˿�������ˮ����
����̼̼˫��������ʹ��ˮ��ɫ��N�к���̼̼˫������ʹ��ˮ��ɫ����˿�������ˮ����![]() ��N����A˵����ȷ��B��E��
��N����A˵����ȷ��B��E��![]() ������̼̼˫������˲���ʹ���Ը��������Һ��ɫ����B˵������C��A�ķ���ʽΪC2H4��
������̼̼˫������˲���ʹ���Ը��������Һ��ɫ����B˵������C��A�ķ���ʽΪC2H4��![]() �ķ���ʽΪC6H12��������ʱ��C2H4��CH2��C6H12��CH2����˵�����ʱ�����ĵ�����������ͬ����C˵����ȷ��D��
�ķ���ʽΪC6H12��������ʱ��C2H4��CH2��C6H12��CH2����˵�����ʱ�����ĵ�����������ͬ����C˵����ȷ��D��![]() ����N��M��MΪ��������˴˷�Ӧ����̼̼˫������N�Ľṹ��ʽ����Ϊ
����N��M��MΪ��������˴˷�Ӧ����̼̼˫������N�Ľṹ��ʽ����Ϊ ��
��![]() ��
��![]() ��
��![]() ����4�֣���D˵������
����4�֣���D˵������


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����д�ʩ�����ӿ�Zn��1mol/LH2SO4��Ӧ����H2�����ʵ���
A. �����¶� B. ��Zn�۴���Zn��
C. ���÷���H2SO4��Zn��Ӧ D. �μ�������CuSO4��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£��������pH��������Ȼ������Һ������˵����ȷ����
A. ����Һ����������ͬ
B. �ֱ��������ҵ�����п��Ӧ��ƽ����Ӧ���ʺ��ߴ�
C. �ֱ����Ũ�ȵ�����������Һ��Ӧ�����ԣ����ĵ��������Ƶ������ͬ
D. ϡ��10���������pH���Ȼ����Һ��pHС
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��4NH3+5O2![]() 4NO+6H2O������Ӧ���ʷֱ���v(NH3)��v(O2)��v(NO)��v(H2O)��mol/(L��min)�ݱ�ʾ������ȷ�Ĺ�ϵʽ��
4NO+6H2O������Ӧ���ʷֱ���v(NH3)��v(O2)��v(NO)��v(H2O)��mol/(L��min)�ݱ�ʾ������ȷ�Ĺ�ϵʽ��
A. 4v(NH3)=5v(O2) B. 5v(O2)=6v(H2O) C. 2v(NH3)=3v(H2O) D. 4v(O2)=5v(NO)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1��������ijͬѧ�Ƶ���1molNa ����������ֵ�ϵ��� Na �����ԭ����������λȡ g���Ĺ� �������㲹�������������� m��Na ԭ������ʾһ�� Na ԭ�ӵ�������m��12C����ʾһ�� 12Cԭ�ӵ����� ��Ar ��ʾ Na �����ԭ��������NA ��ʾ�����ӵ�������
��Ϊ��m��Na ԭ����=1/12m��12C��Ar��������1molNa ԭ�ӵ�����=1/12________Ar=1/12_____ Ar=Ar g
��2���� CO2 �� CO ��ɵĻ������� H2 ������ܶ� 20������������ CO2 ���������Ϊ_____��CO ����������_______
��3����״������336L �� NH3 ���� 1L ˮ����������Һ���ܶ�Ϊ ag/cm3���������ʵ���Ũ��Ϊ����������ˮȫ��ת��Ϊ NH4CL������ 2mol/L ����������Ϊ_____��NH3��HCl=NH4Cl����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2002��12��ij�գ���ij�����̱����ŷ������ϣ������Ƴ�������������ע���̱��ٻ������̱ꡣ�þƳ�������һ�ְƴ���Ũ�����ǩ�ϱ���55��������������ʾ�� ��
A. �þ������¶�Ϊ55���������������
B. ���˸þƺ��������¶ȿɴ�55��
C. �þƵķе�Ϊ55��
D. �þ����Ҵ��ĺ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ȼ�����Ʒ����������Na2SO4 �� Na2CO3�����������̽��о��������������е�( )��д�Ϻ��ʵ��Լ�����[ ]��д��ʵ���������:______,______,______,______,______,______,______��
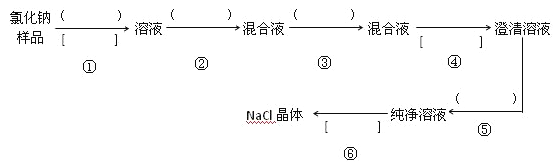
д���йط�Ӧ�Ļ�ѧ����ʽ:
�ڢڲ���______________________, _________________________��
�ڢ۲���______________________��
�ڢݲ���______________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NA��ʾ�����ӵ�������������˵����ȷ���ǣ� ��
A. 0.1 mol/L K2SO4��Һ����K+ 0.2NA
B. ��״���£�11.2Lˮ�����ĵ�����Ϊ5NA
C. ���³�ѹ�£�16g O2��������Ϊ10NA
D. 0.1 mol Mgԭ�ӱ��Mg2+ʱʧȥ�ĵ�����Ϊ0.2NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA��ʾ�����ӵ�����������˵���У���ȷ������ ��
A. 1 mol Cl2��Ϊ�������õ��ĵ�����ΪNA
B. ��0 �棬101 kPaʱ��22.4 L�����к���NA����ԭ��
C. 25 �棬1.01��105Pa��64 g SO2�к��е�ԭ����Ϊ3NA
D. ��0.1 mol FeCl3�ӵ���ˮ���ƵõĽ����У�������0.1NA
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com