
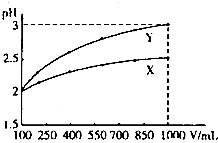
| A、X为弱酸,VX<VY |
| B、Y为强酸,VX>VY |
| C、X为强酸,VX>VY |
| D、Y为弱酸,VX>VY |
科目:高中化学 来源: 题型:
| A、氯化亚铁溶液中通入氯气:Fe2++Cl2═Fe3++2C1- |
| B、金属钠投入水中Na+H2O═Na++OH-+H2↑ |
| C、铝粉投入到NaOH溶液中:2Al+2OH-═2AlO2-+H2↑ |
| D、氯化铁溶液中加氨水3NH3?H2O+Fe3+=3NH4++Fe(OH)3↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、无论是风力发电还是潮汐发电,都是将化学能转化为电能 |
| B、光缆在信息产业中有广泛应用,制造光缆的主要材料是单质硅 |
| C、推广燃煤脱硫技术,可以防治SO2污染 |
| D、凡含有食品添加剂的食物对人体健康均有害,不宜食用 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| 序号 | 反应 | 平衡常数 |
| 1 | Au+6HNO3(浓)═Au(NO3)3+3NO2↑+3H2O | <<1 |
| 2 | Au3++4Cl-═AuCl4- | K |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、C的体积分数下降 |
| B、a+b>p |
| C、正反应速率和逆反应速率均减小,平衡向逆反应方向移动 |
| D、正反应速率和逆反应速率均加大,平衡向正反应方向移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、同浓度下列溶液中:①(NH4)2SO4 ②NH4HCO3 ③NH4Cl④NH3?H2O,C(NH4+)由大到小的顺序是:①>③>②>④ |
| B、常温时,将等体积的盐酸和氨水混合后,pH=7,则C(NH4+)>C (Cl-) |
| C、0.2 mol/LNa2CO3溶液中:C (OH-)=C (HCO3-)+C (H+)+C (H2CO3) |
| D、同浓度的下列溶液中,①NaCl ②Na2CO3 ③CH3COONa④NaOH,pH值由大到小的顺序是:④>③>②>① |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com