
| ||
| ||
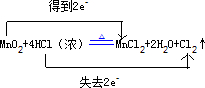 ,故答案为:MnO2;
,故答案为:MnO2; .
.

 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案科目:高中化学 来源:不详 题型:单选题
| A.因为反应放热,所以升高温度会使反应速率减慢 |
| B.通过调控反应条件,SO2可以100%地转化为SO3 |
| C.当SO2与SO3的浓度相等时,反应达到平衡 |
| D.使用催化剂的目的是加快反应速率,提高生产效率 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| V2O5 |
| △ |
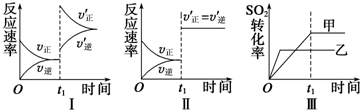
| A.图Ⅰ表示的是t1时刻增大O2的浓度对反应速率的影响 |
| B.图Ⅱ表示的是t1时刻加入催化剂后对反应速率的影响 |
| C.图Ⅲ表示的是催化剂对化学平衡的影响,且甲的催化效率比乙高 |
| D.图Ⅲ表示的是压强对化学平衡的影响,且乙的压强较高 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.升高温度,正反应速率减小,逆反应速率增加,平衡逆向移动 |
| B.升高温度,可提高CO2转化率 |
| C.增加H2的浓度,可提高CO2转化率 |
| D.改用高效催化剂,可增大反应的平衡常数 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Fe2(SO4)3=2Fe+3+3SO4-2 | B.CuCl2=Cu2++Cl2- |
| C.NaOH=Na++OH- | D.Ba(NO3)2=Ba2++2(NO3)2- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.NaHCO3═Na++HCO3- | B.H2SO4═2H++SO42- |
| C.MgCl2═Mg2++2Cl- | D.NH3?H2O═NH4++OH- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.常温下,0.1 mol·L-1 CH3COOH溶液的pH=1 |
| B.铅蓄电池在放电过程中,负极质量增加,正极pH减少 |
| C.反应CO2(g)+C(s)=2CO(g)在低温下不能自发进行,则其△H>0 |
| D.常温下,向AgCl浊液中加入少量NaCl饱和溶液,则c(Ag+)、Ksp(AgCl)均减小 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com