
【题目】离子方程式BaCO3+2H+=CO2↑+H2O+Ba2+中的H+能代表的物质是( )
①HCl ②H2SO4 ③HNO3 ④NaHSO4 ⑤CH3COOH
A. ②④⑤ B.①④⑤ C.①⑤ D.①③
 小学课时特训系列答案
小学课时特训系列答案科目:高中化学 来源: 题型:
【题目】碳及其化合物在能源、材料等方面具有广泛的用途。回答下列问题:
(1)碳酸和草酸均为二元弱酸,其电离分为两步进行,已知其电离常数的有关数据如下表:向Na2CO3溶液中滴加草酸溶液,开始时所发生反应的离子方程式为 。
H2CO3 | H2C2O4 | |
K1 | 4.2×10-7 | 5.4×10-2 |
K2 | 5.6×10-11 | 5.4×10-5 |
(2)常温时,C和CO的燃烧热△H分别为-394.0 kJ·mol-1、-283.0 kJ·mol-1,该条件下C转化为CO的热化学方程式为 。
(3)氢气和一氧化碳在一定条件下可合成甲醇,反应如下
2H2(g)+CO(g)![]() CH3OH(g) △H=Q kJ·mol-1。
CH3OH(g) △H=Q kJ·mol-1。
①该反应在不同温度下的化学平衡常数(K)如下表:
温度(℃) | 250 | 300 | 350 |
K(L2·mol-1) | 2.041 | 0.270 | 0.012 |
由此可判断Q 0(填“>”、“=”或“<”)
②一定温度下,将6 mol H2和2mol CO充入到体积为2 L的密闭容器中,10 min时反应达到平衡状态,此时测得c(CO)=0.2 mol·L-1,该温度下的平衡常数K= 。0~10 min内,反应速率v(CH3OH)= 。
③在两个密闭容器中分别都充入20 mol H2和10 mol CO,测得一氧化碳的平衡转化率随温度(T)、压强(p)的变化如下图所示:
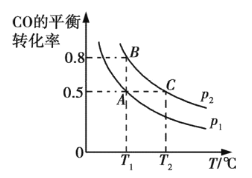
A、B两点压强大小关系:p1 p2(填“>”、“=”或“<”)。若A点对应容器的容积为20 L,则B点对应的容器的容积为 L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将燃煤废气中的CO2转化为二甲醚的反应原理为:2CO2(g)+6H2(g)![]() CH3OCH3(g)+3H2O(g),一定条件下,现有两个体积均为1.0L恒容密闭容器甲和乙,在甲中充入0.1molCO2和0.2molH2,在乙中充入0.2molCO2和0.4molH2,发生上述反应并达到平衡。该反应中CO2的平衡转化率随温度的变化曲线如图所示。下列说法正确的是
CH3OCH3(g)+3H2O(g),一定条件下,现有两个体积均为1.0L恒容密闭容器甲和乙,在甲中充入0.1molCO2和0.2molH2,在乙中充入0.2molCO2和0.4molH2,发生上述反应并达到平衡。该反应中CO2的平衡转化率随温度的变化曲线如图所示。下列说法正确的是

A.反应2CO2(g)+6H2(g)![]() CH3OCH3(g) + 3H2O(g)的 △S<0、△H<0
CH3OCH3(g) + 3H2O(g)的 △S<0、△H<0
B.表示乙容器CO2的平衡转化率随温度变化的是曲线B
C.体系中c(CH3OCH3):c(CH3OCH3,状态Ⅱ)<2c(CH3OCH3,状态Ⅲ)
D.逆反应速率v逆:v逆(状态Ⅰ)<v逆(状态Ⅲ)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中,正确的是( )
A. 活化分子间的碰撞一定是有效碰撞
B. 其他条件相同时,增大反应物浓度,反应物中活化分子的百分数增加
C. 焓变和熵变都与反应的自发性有关,它们都能独立地作为自发性的判据
D. 常温下,FeCl3溶液中由水电离出的c (H+)一定大于1×10﹣7mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列电离方程式中,正确的是
A. Na2SO4=2Na++S04-2 B. Ba(OH)2=Ba2++OH-2
C. Al2(SO4)3=2A13++3SO42- D. Ca(N03)2=Ca2++2(N03) 2-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组混合物的分离或提纯方法不正确的是( )
A.用加热法分离碘和氯化铵的混合物(提示:碘易升华,氯化铵受热易分解,冷却后它们又都重新生成原固体)
B.用结晶法提纯NaCl和KNO3混合物中的KNO3
C.用蒸馏法分离乙醇和水的混合物
D.用分液的方法分离煤油和NaCl溶液的混合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ、前20号主族元素A、B、C、D、E、F的原子序数依次增大,它们的原子核最外层电子数之和为18。A的原子半径为自然界最小,B、F为同一主族,E为地壳中含量最多的金属元素,F原子的最外层与最内层电子数相等。C、D可以形成两种常见化合物。试回答以下问题:
(1)写出C与F元素形成的化合物的电子式
(2)A、C、D三种元素形成的化合物C2A4D2中一定含有 。(填“离子键”、“极性共价键”或“非极性共价键”)
(3)由D、E、F形成的简单离子的离子半径由大到小的顺序是 。(用元素离子符号表示)
(4)元素B的性质与元素E的性质很相似,试写出以下反应的离子方程式:
B的氧化物与氢氧化钠溶液反应:
Ⅱ、现有A、B、C、D四种短周期元素,A分别与B、C、D结合生成甲、乙、丙三种化合物,且甲、乙、丙三分子均为10电子粒子,C、D结合生成化合物丁。有关元素的单质和甲、乙、丙、丁四种化合物的转化关系如下图所示:

(1)根据以上条件可以确定A、B、C、D四种元素中的三种元素。不能被确定的第四种元素是________。(填写A B C D中的一种)
(2)依据下列条件可以进一步确定上述第四种元素:①甲与丙以及乙与丙均能够发生反应 ②甲、丙都是无色、有刺激性气味的物质。据此,写出C+丙―→乙+丁的化学反应方程式___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“酸雨”的形成主要是由于( )
A.森林遭到乱砍滥伐,破坏了生态平衡 B.工业上大量燃烧含硫燃料
C.汽车排出大量的尾气 D.大气中二氧化碳含量增多
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com