
| A.①② | B.②③ |
| C.③④ | D.②④ |
科目:高中化学 来源:不详 题型:单选题
| A.苯中含有苯酚杂质:加入溴水,过滤 |
| B.乙醇中含有乙酸杂质:加入碳酸钠溶液,分液 |
| C.FeCl3溶液中含有CuCl2杂质:加入过量铁粉,过滤 |
| D.CO2中含有HCl杂质:通入饱和NaHCO3溶液,洗气 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
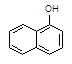 +C2H5OH
+C2H5OH
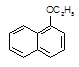 +H2O
+H2O

| 实验目的 | 实验操作 | 预期现象和结论 |
| ①用金属钠检验1-乙氧基萘是否纯净 | 取少量经提纯的产品于试管A中,加入金属钠 | 若 ,则产品纯净; 若 ,则产品不纯。 |
| ②检验经提纯的产品是否含有1-萘酚 | | 若 ,则含有1-萘酚; 若 ,则不含1-萘酚。 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.HCl、CuSO4、Mg(NO3)2、KOH | B.NaBr、AgNO3、HCl、Na2CO3 |
| C.H2SO4、NaCl、Na2SO4、Na2CO3 | D.NaOH、MgSO4、Na2CO3、KHSO4 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.新制碱性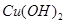 悬浊液 悬浊液 | B.FeCl3溶液 |
| C.BaCl2溶液 | D.酸性KMnO4溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
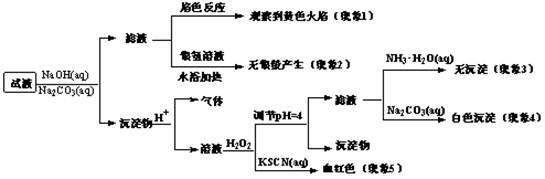
| A.根据现象1可推出该试液中含有Na+ |
| B.根据现象2可推出该试液中并不含有葡萄糖酸根 |
| C.根据现象3和4可推出该试液中含有Ca2+,但没有Mg2+ |
| D.根据现象5可推出该试液中一定含有Fe2+ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com