
【题目】下列分类中不正确的是
A. 依据分子组成中含有氢原子的数目,将酸分为一元酸、二元酸等
B. 依据是否有电子转移,将化学反应分为氧化还原反应和非氧化还原反应
C. 依据在水溶液中或熔融状态下是否导电,将化合物分为电解质和非电解质
D. 依据组成元素的种类,将纯净物分为单质和化合物
 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:高中化学 来源: 题型:
【题目】化合物G对多种植物病原菌具有抑制作用,由丙酮合成G的路线如下: 
(1)写出化合物G中含氧官能团的名称 .
(2)反应②的类型为 .
(3)反应①还会得到另一产物H,其分子式为C8H14O2 , 写出H的结构简式 .
(4)反应⑦生成的G会部分转化为另一产物I,Ⅰ为链状结构,分子式为C10H18O4 , 写出Ⅰ的结构简式:
(5)一分子G消去一分子水可得物质J,写出同时满足下列条件的J的一种同分异构体的结构简式: ①能与FeCl3溶液发生显色反应;②分子的核磁共振氢谱有2个峰.
(6)以CH3OH、CH≡CH为原料合成聚丙烯醇 ![]() ,写出合成流程图(无机试剂任用).合成流程图示例如下:CH2=CH2
,写出合成流程图(无机试剂任用).合成流程图示例如下:CH2=CH2 ![]() CH3CH2Br
CH3CH2Br ![]() CH3CH2OH.
CH3CH2OH.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】难溶电解质在水溶液中存在着电离平衡.在常温下,溶液里各离子浓度以它们化学计量数为方次的乘积是一个常数,叫溶度积常数(Ksp).例如:Cu(OH)2 ![]() Cu2++2OH﹣ , Ksp=c(Cu2+)[c(OH﹣)]2=2×10﹣20 . 当溶液中各离子浓度方次的乘积大于溶度积时,则产生沉淀,反之固体溶解.
Cu2++2OH﹣ , Ksp=c(Cu2+)[c(OH﹣)]2=2×10﹣20 . 当溶液中各离子浓度方次的乘积大于溶度积时,则产生沉淀,反之固体溶解.
(1)某CuSO4溶液里c(Cu2+)=0.02mol/L,如果生成Cu(OH)2沉淀,应调整溶液pH,使之大于 .
(2)要使0.2molL﹣1CuSO4溶液中Cu2+沉淀较为完全(使Cu2+浓度降至原来的千分之一)则应向溶液里加NaOH溶液,使溶液pH值为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知和碳元素同主族的X元素位于周期表中的第1个长周期,短周期元素Y原子的最外层电子数比内层电子总数少3,它们所形成化合物的分子式是XY4。试回答:
(1)X元素的原子基态时电子排布式为__________;Y元素原子最外层电子的电子排布图为__________。
(2)若X、Y两元素电负性分别为2.1和2.85,则XY4中X与Y之间的化学键为__________(填“共价键”或“离子键”)。
(3)该化合物的立体构型为__________,中心原子的杂化类型为__________,分子为__________(填“极性分子”或“非极性分子”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将下图中所列仪器组装为一套实验室蒸馏石油的装置,并进行蒸馏,得到汽油和煤油。
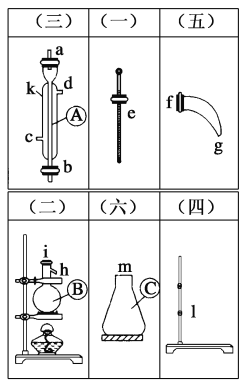
(1)图中A、B、C三种仪器的名称是______________________。
(2)将以下(一)~(六)中的仪器,用字母a、b、c……表示连接顺序:
e接( );( )接( );( )接( );( )接( );( )接( )。
(3)A仪器中c口用于____________,d口用于____________。
(4)蒸馏时,温度计水银球应处在____________位置。
(5)在B中注入原油后,加几片碎瓷片的目的是_______________________。
(6)给B加热,收集到沸点为60 ℃~150 ℃间的馏分是________,收集到沸点为150 ℃~300 ℃间的馏分是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】羰基硫(COS)可作为一种粮食熏蒸剂,能防止某些昆虫、线虫和真菌的危害.在恒容密闭容器中,将CO和H2S混合加热并达到下列平衡:CO(g)+H2S(g)COS(g)+H2(g),K=0.1,反应前CO的物质的量为10mol,平衡后CO物质的量为8mol,下列说法正确的是( )
A.升高温度,H2S浓度增加,表明该反应的△H>0
B.随着反应的进行,混合气体的密度逐渐减小
C.反应前H2S物质的量为7mol
D.CO的平衡转化率为80%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列操作中正确的是
A. 用蒸发方法使NaCl从溶液中析出时,将蒸发皿中NaCl 溶液全部加热蒸干
B. 在托盘天平上称量NaOH时,应将NaOH固体放在小烧杯中称量
C. 用25 mL量筒量取4.0 mol/L的盐酸5.62 mL
D. 用托盘天平准确称取5.85 g NaCl固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(多选)FeCl3(aq)与KSCN(aq)混合时存在下列平衡:Fe3+ (aq)+SCN﹣(aq) ![]() Fe(SCN)2+ (aq);已知平衡时,物质的量浓度c[Fe(SCN)2+]与温度T的关系如下图所示,则下列说法正确的是( )
Fe(SCN)2+ (aq);已知平衡时,物质的量浓度c[Fe(SCN)2+]与温度T的关系如下图所示,则下列说法正确的是( ) 
A.FeCl3(aq)与KSCN(aq)反应的热化学反应方程式为:Fe3+(aq)+SCN﹣(aq)=Fe(SCN)2+(aq)△H>0
B.温度为T1、T2时,反应的平衡常数分别为K1、K2 , 则K1>K2
C.反应处于D点时,一定有V正>V逆
D.A点与B点相比,A点的c(Fe3+)大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com