
【题目】下列条件下,两瓶气体所含原子数一定相等的是( )
A.同质量、不同密度的N2和CO
B.同温度、同体积的H2和N2
C.同体积、同密度的N2和CO2
D.同压强、同体积的N2O和CO2
【答案】A
【解析】A、由N=nNA= ![]() NA知,两种气体的质量相同,摩尔质量相同,所以所含分子数相同,且氮气和一氧化碳都是双原子分子,所以含有的原子数相同,故A符合题意;
NA知,两种气体的质量相同,摩尔质量相同,所以所含分子数相同,且氮气和一氧化碳都是双原子分子,所以含有的原子数相同,故A符合题意;
B、气体体积受温度压强的影响,同温同体积的H2和N2 , 因为压强未知,所以两种气体的物质的量不一定相同,所含分子数不一定相同,导致所含原子数不一定相同,故B不符合题意;
C、同体积同密度的N2和CO2 , 两种气体的质量相同,N=nNA= ![]() NA知分子数目不相同,所含原子数不相同,故C不符合题意;
NA知分子数目不相同,所含原子数不相同,故C不符合题意;
D、气体体积受温度压强的影响,因为温度未知,所以同压同体积的N2O和CO2 , 两种气体的物质的量不一定相等,所含分子数不一定相等,导致所含原子数不一定相等,故D不符合题意;
故选A。


 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案科目:高中化学 来源: 题型:
【题目】设NA为阿伏伽德罗常数的值.下列说法正确的是( )
A.高温下,0.2 mol Fe与足量水蒸气反应,生成的H2分子数目为0.3NA
B.室温下,1 L pH=13的NaOH溶液中,由水电离的OH﹣离子数目为0.1NA
C.氢氧燃料电池正极消耗22.4 L(标准状况)气体时,电路中通过的电子数目为2NA
D.5NH4NO3 ![]() 2HNO3+4N2↑+9H2O反应中,生成28 g N2时,转移的电子数目为3.75NA
2HNO3+4N2↑+9H2O反应中,生成28 g N2时,转移的电子数目为3.75NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生产上用过量烧碱溶液处理某矿物(含Al2O3、MgO),过滤后得到滤液用NaHCO3溶液处理,测得溶液pH和Al(OH)3生成的量随加入NaHCO3溶液体积变化的曲线如下:下列有关说法不正确的是( ) 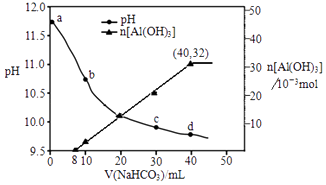
A.NaHCO3溶液的物质的量浓度为0.8 mol/L
B.b点与c点溶液所含微粒种类相同
C.a点溶液中存在的离子是Na+、AlO2﹣、OH﹣、H+
D.生成沉淀的离子方程式为:HCO3﹣+AlO2﹣+H2O═Al(OH)3↓+CO32﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学点亮生活。下列说法中,不正确的是
A. 沙子是基本的建筑材料B. 光导纤维的主要成分是硅
C. 硅酸钠是制备木材防火剂的原料D. 目前制作太阳能电池板的材料是硅
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】火药是中国的“四大发明”之一,永远值得炎黄子孙骄傲,也永远会激励着我们去奋发图强。黑火药在发生爆炸时,发生如下的反应:2KNO3+3C+S=K2S+N2↑+3CO2↑。
(1)其中被还原的元素是 , 被氧化的元素是 , 氧化剂是 , 还原剂是 , 氧化产物是 , 还原产物是。
(2)用双线桥标出电子转移的方向和数目:2KNO3+ 3C+ S ═ K2S + N2↑+ 3CO2↑。
(3)当0.1molCO2生成时,则转移的电子数为个。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机物说法正确的是( )
A. 植物油、裂化汽油均能使酸性高锰酸钾褪色B. 糖类、油脂、蛋白质在一定条件下均能水解
C. CH3CH==CH2所有原子共平面D. 化学式C2H4O2表示的物质一定是纯净物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CuCl2、CuCl广泛用于有机合成的催化剂.CuCl2容易潮解; CuCl白色粉末,微溶于水,溶于浓盐酸和氨水生成络合物,不溶于乙醇. 已知:i.CuCl2+Cu+2HCl(浓)2H[CuCl2](无色) ![]() 2CuCl↓(白色)+2HCl
2CuCl↓(白色)+2HCl
ii.副反应:CuCl+H2OCuOH+2HCl; CuCl+Cl﹣═[CuCl2]﹣
(1)制取CuCl2装置如图: 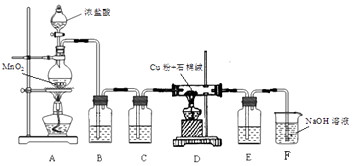
①A装置中发生反应的离子方程式是 .
②C、E 装置中盛放的是浓硫酸,作用是 .
③B中选择饱和食盐水而不用蒸馏水的原因是 .
(2)制取CuCl流程如图: 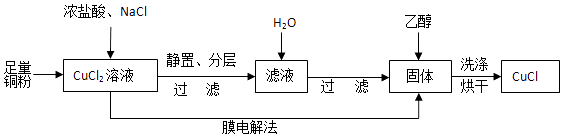
①反应①中加入NaCl的目的是;但是Cl﹣浓度过高,CuCl产率降低,原因是 .
②CuCl在潮湿的环境中易被氧化为Cu2(OH)3Cl,反应的方程式为 .
③利用膜电解法制取CuCl,阴极电极反应式为 .
④用乙醇洗涤沉淀Y的原因为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分枝酸可用于生化研究.其结构简式如图.下列关于分枝酸的叙述正确的是( ) 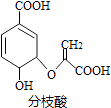
A.分子中含有2种官能团
B.可与乙醇、乙酸反应,且反应类型相同
C.1mol分枝酸最多可与3molNaOH发生中和反应
D.可使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色,且原理相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电子工业中用过量的FeCl3溶液溶解电路板中的铜箔时,会产生大量废液.由该废液回收铜并得到净水剂(FeCl36H2O)的步骤如下:
Ⅰ.在废液中加入过量铁粉,过滤;
Ⅱ.向I的滤渣中加入过量试剂A,充分反应后,过滤,得到铜;
Ⅲ.合并Ⅰ和Ⅱ中的滤液,通入足量氯气;
Ⅳ.…,得到FeCl36H2O晶体.
(1)用FeCl3溶液腐蚀铜箔的离子方程式是 .
(2)试剂A是 .
(3)步骤Ⅲ中发生的离子方程式为 .
(4)完成步骤Ⅳ需要用到的实验装置是(填字母). 
(5)若用FeCl36H2O晶体配制100ml 0.5mol/L的FeCl3溶液
①用托盘天平称FeCl36H2O晶体,其质量是g.
②实验时下图所示操作的先后顺序为(填编号).
蒸馏水
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com