
 ��ͼ��ʾ����ʯī���缫�ĵ����У�����500mL��һ�����ʵ�ij��ɫ��Һ���е�⣬�۲쵽A�缫�����к�ɫ�����������ɣ�B�缫�л���ɫ�������ɣ���ʹ���۵⻯����Һ����������Һ�е�ԭ��������ȫ����ֹͣ��⣬ȡ��A�缫��ϴ�ӡ�����������缫����1.6g���ش��������⣮
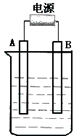
��ͼ��ʾ����ʯī���缫�ĵ����У�����500mL��һ�����ʵ�ij��ɫ��Һ���е�⣬�۲쵽A�缫�����к�ɫ�����������ɣ�B�缫�л���ɫ�������ɣ���ʹ���۵⻯����Һ����������Һ�е�ԭ��������ȫ����ֹͣ��⣬ȡ��A�缫��ϴ�ӡ�����������缫����1.6g���ش��������⣮���� ��1���͵�Դ�ĸ����������ǵ��ص��������͵�Դ�������������ǵ��ص�������
��2���������Ե�ͭ�ε�ʵ���ǵ���κ�ˮ�����ݵ缫��Ӧ��д��ⷽ��ʽ��
��3�����ݵ���������Һ�������ӵ�Ũ�ȼ�����Һ��pH��������Һ��ԭ����ѭ��ԭ���ǣ���ʲô��ʲô������Ԫ���غ��������������ʵ�������
��4�����ݵ��صĹ����Լ��缫��Ӧʽ���㣮
��� �⣺��1�����Һ����ɫ��Һ��A�缫�����к�ɫ�Ĺ�̬�������ɣ�����A����ͭ���ӵõ��ӣ�����A����������A�ӵ��ǵ�Դ�ĸ�����B�缫����ɫ�������ɣ���һ����������ʧ���Ӳ���������������B�Ǹ�װ���������͵�Դ�������������ʴ�Ϊ������
��2��A����������������Ӧ��2Cu2++4e-=2Cu��B�缫��������������Ӧ��4OH--4e-=2H2O+O2�������ʱ��Ӧ�������ӷ���ʽΪ��2Cu2++2H2O$\frac{\underline{\;ͨ��\;}}{\;}$2Cu+4H++O2�����ʴ�Ϊ��2Cu2++4e-=2Cu��4OH--4e-=2H2O+O2����2Cu2++2H2O$\frac{\underline{\;ͨ��\;}}{\;}$2Cu+4H++O2����
��3��ȡ��A�缫��ϴ�ӡ�����������缫����1.6g������������������ͭ��������1.6g����0.025mol�����ݵ缫��Ӧ��Cu2++2e-��Cu��B�缫��ʧȥ���Ӻõ缫�ϵõ��ĵ���һ���࣬��ʧȥ������0.05mol����Ŀ��0.05NA���������������ӵ����ʵ���Ϊ0.05mol������c��H+��=$\frac{0.05mol}{0.5L}$=0.1mol/L����pH=1��
�ʴ�Ϊ��0.05NA��1��
��4�����ֵ��Һ���䣬��A��B�缫�ֱ��������ͭ�缫����ʱ����Cu��������������Ӧ�ĵ缫����ʽΪ��Cu-2e-=Cu2+�����������ᣬFe���������õ缫������ͭ���ʣ��������ӣ������̣�ˮ������ŵ磬������Һ��pH���䣬
�ʴ�Ϊ��������ɫ���ʣ��缫�������Cu-2e-=Cu2+�����䣮
���� ���⿼��ѧ�����صĹ���ԭ����ע��缫��Ӧ����д�Լ������غ�ļ����ǹؼ����ѶȲ���


 ���б�ˢ��ϵ�д�
���б�ˢ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

 ��
�� ��
�� ��
�� ���������֣���
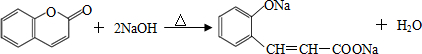
���������֣��� ��CH3CHO�ܷ������Ʒ�Ӧ�١��ڵ�������Ӧ���������ɵ��л���Ľṹ��ʽΪ
��CH3CHO�ܷ������Ʒ�Ӧ�١��ڵ�������Ӧ���������ɵ��л���Ľṹ��ʽΪ ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
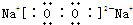 �����к��еĻ�ѧ������Ϊ���Ӽ����Ǽ��Լ�
�����к��еĻ�ѧ������Ϊ���Ӽ����Ǽ��Լ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �������Ľṹ��ʽ�� | B�� | CO2���ӱ���ģ�ͣ� | ||
| C�� | NH4Cl�ĵ���ʽ�� | D�� | NaCl�ľ���ģ�ͣ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �� | B�� | �ڢ� | C�� | �ڢۢ� | D�� | �٢ڢۢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ��ѧ�� | C-H | C-F | H-F | F-F |
| ����/��kJ•mol-1�� | 414 | 489 | 565 | 155 |
| A�� | ���� 1940 kJ | B�� | ���� 1940 kJ | C�� | ���� 485 kJ | D�� | ���� 485 kJ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com